剂型与疗效
药物必须以一定的剂型使用。药物所产生的生物效应除受本身特有的药理作用支配外,还受到生物体和剂型因素的影响。这些影响的总的结果使药物的起效时间、作用强度和持续时间常有很大的差异。剂型因素对疗效的影响有时表现得十分突出,合理设计并制造的剂型,能够大大增进疗效,减少毒副作用。
Wagner(1961)首先提出生物药剂学指出其任务是研究“药物及其剂型的理化性状与用药后(用药物的不同剂型)观察到的生物效应之间的相互关系”。由此可知,剂型与疗效是它的主要研究任务。剂型一词,在此不应局限于传统意义上的那些剂型如丸、片、胶囊剂等,还应更广泛地包括药物的理化性状如粉末粒度的大小,结晶形态以及药物的化学形式如游离酸(碱)或盐、或酯或其他复合物等。
药物的治疗作用与药物在血液中或其他分布液中的浓度有关,例如苯妥因在血浆中的安全有效的治疗浓度为10~20μg/ml。所以,制剂的血药浓度与其随时间的变化规律常可用以判断该剂型的疗效如何。以口服给药为例,服用固体药剂后药物从剂型中溶出而吸收,在吸收的同时进行着药物的体内分布和排除过程。吸收过程和排除过程相比较,前者速度常可数倍于后者。随着时间的延长,药物在血浆中的浓度逐渐升高,到吸收完成时,血药浓度即渐渐下降,如图1所示。血药浓度到达有效水平所需的时间称为起效时间,血药水平保持在有效水平以上的时间称为持续时间,从有效水平到最高点的距离称为作用强度。药物吸收速度与排除速度的快慢,是药物本身决定的,但剂型因素可以在很大程度上改变药物的吸收速度,而一般不影响药物的排除速度。所以排除速度保持不变。因此,同一药物的不同剂型,尽管给药途径、剂量都相同,但可以产生如图2所示的几种不同的血药浓度-时间曲线。曲线Ⅰ、Ⅱ、Ⅲ的尾部平行,说明它们的排除速度常数Ke不变,但吸收速度常数Ka从曲线Ⅰ到曲线Ⅲ顺序减小。Ka的减小导致血药浓度顶点(峰值Cm) 的下降与达到峰值的时间tm的延长。剂型Ⅰ起效时间快,作用强度大,持续时间短。剂型Ⅱ起效时间长,作用强度小,持续时间长。剂型Ⅲ任何时间都低于有效水平。图2概括地说明了剂型因素对疗效影响的严重程度。由于治疗上的不同需要,有时要求以曲线Ⅰ代表的剂型,有时则要求以曲线Ⅱ代表的剂型,也有要求兼具曲线Ⅰ、Ⅱ的优点而摒除它们各自缺点的剂型。要达到上述要求,必须研究影响药物从剂型中释放、溶解及吸收的速度和程度的一系列因素。这些因素主要分为两大类。即药物的理化性状的影响和剂型因素的影响。
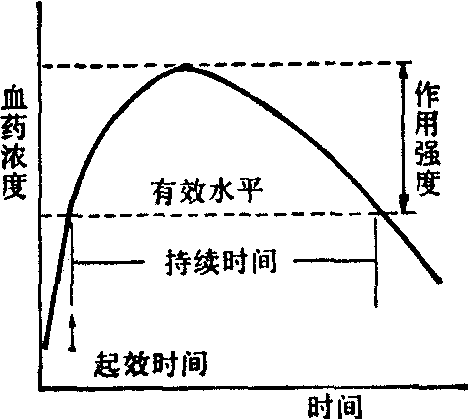
图1 血药浓度-时间曲线与药理
效应的关系
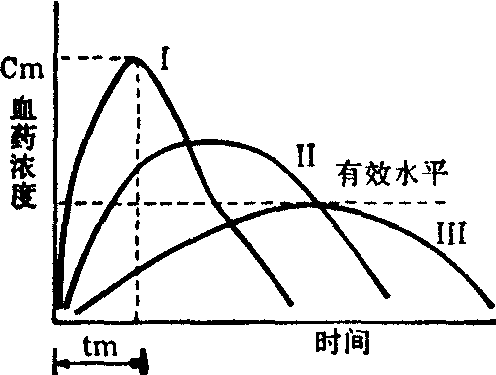
图2 三种不同剂型药物的血药
浓度-时间图象
在讨论药物理化性状对吸收的影响时,有重要意义的是如何增进一些难溶于水的药物的吸收问题。Noyes-Whitney溶出速度方程(见“溶出速度”条)概括了影响药物溶出速度dC/dt的一些因素。很多研究表明,体外溶出速度与体内吸收有较好的相关,因此改善难溶性药物的吸收可以从提高它的体外溶出速度着手。S增大可获得较快的溶出速度。灰黄霉素、安体舒通等药物得以成功地使用,都是由于增大S,使药粉微粒化或更进一步利用固体分散法使成为更加细小的微粒而充分发挥了它们的疗效。其他药物如氯霉素、磺胺嘧啶等都可借增大表面积S来增进药物的吸收。增大溶解度Cs也是导致较快吸收的一种措施,以难溶性弱酸性药物为例,可采用它的可溶性盐,或以碱性物质与该弱酸药物混合,以改变药粒周围介质的pH值,从而增大溶出速度,使吸收改善。所用的碱性物质的量,并不足以改变整个介质的pH,但因药粒周围介质pH上升,溶解度增大,虽在总体介质中因pH下降而使该酸性药物回复到难溶性酸而析出,但此时的粒子极细,根据Noyes-Whitney方程,其溶出速度有所增加,故仍然有利于吸收,例如缓冲阿斯匹林片即为一例。弱酸可溶性盐的吸收情况的改善,其原因也相同。例如新生霉素盐的溶解度较其本身游离酸大50倍,体内生物利用度则增大一倍。溶解度增大,虽然常可相应增大溶出速度,但并非都如此。这是因为胃肠道的吸收进行得很快,故药物往往等不到溶解到饱和程度才被吸收,所以重要的是溶出的速度要快,才能保证良好的吸收。药物有时存在着同质多晶体或无定形。同质多晶体中的亚稳定晶型以及无定形粉末一般有较大的溶解度,具有较好的疗效。如甲基泼尼松晶体Ⅱ的溶解度较晶体Ⅰ大,溶出速度也大1.4倍,吸收速度大1.7倍(大白鼠)。无定形的新生霉素在0.1 NHCl的溶解度较结晶形的大10倍,故生物效应也很明显,它产生的血药浓度为同剂量钠盐的两倍。与同质多晶相类似的,是一些化合物含有或不含结晶水时也有溶解度的差别。无水物有较大的溶解度,例如茶碱、咖啡碱、导眠能、氨苄青霉素等。也有相反的情况,例如苯巴比妥的一水化合物的溶解度大于无水物。
快速溶出并不是任何情况都需要的,副作用很大的呋喃坦啶的粒度应当不小于200目筛,否则呕吐副作用的发生率增大,粒度过大则疗效变差,故通常最好在80目筛到200目筛之间。对于在胃酸中不稳定的药物,快速溶出只能加速降解而降低了它的生物利用度。例如在胃酸中极不稳定的红霉素,吸收最好最多的却是溶出速度最小的红霉素丙酸酯。
在剂型因素对吸收的影响方面,一般说来主要也取决于药物的释放速度。通常,药物的吸收速度按下列顺序减少: 溶液剂>混悬剂>胶囊剂>压制片 (相等或不相等)>包衣片。
溶液剂 药物以水溶液形式应用时,胃肠吸收最快。但由于一系列原因如稳定性、恶味、服用不便等常使溶液剂的应用受到限制。酸性胃液对药物溶液的稀释常可导致沉淀,但析出的粒子极细,故仍可很快溶解吸收。药物在可被体液混合的非水溶剂中的吸收,也较固体剂型为快。但在不能被体液混合的溶剂中,例如油中溶解的药物,其吸收较水溶液中的药物少而慢。油中药物从油相向水性体液的分配过程常是吸收过程中的限速过程。虽然如此,乳剂中药物的吸收一般仍较水性混悬剂中的药物吸收为快。
混悬剂 药物释放速度仅次于溶液剂,因为它的分散界面很大。设计混悬剂处方时需考虑药物粒子的大小,是否有不吸收的复合物形成等情况。后者如苯丙胺与助悬剂羧甲基纤维素钠可形成难溶性复合物而难于吸收。此外尚应考虑同质多晶体,粘度等问题。
胶囊剂 药物从胶囊中的吸收速度很大程度上取决于剂型因素,其中包括粘度大小,与其他药物或辅料是否可能发生相互影响等。例如有人对四批氯霉素胶囊进行体内外试验,发现有一批胶囊体外溶出测定三小时后胶壳虽已溶去,但囊内药物仍保持原来形状而不分散。这几批胶囊的体内血药浓度,以相同剂量比较也相差很大。在对青霉素钠盐胶囊的研究中,也发现由于滑润剂不同,各批之间药物溶出速度差异很大。胶囊剂的药物吸收一般较片剂为快,但也有例外的情况,不能一概而论。
片剂 片剂是最常用的剂型,但药物吸收常较慢且不完全。主要是因为药物在颗粒中被紧压,有效表面积减少,药片与体液接触后如果不能迅速崩解并同时将其中药物溶出(图3),则其生物利用度就会受到严重影响。崩解对于绝大多数药物的吸收是很重要的,如果片剂不能崩解或崩解很差,则药物的溶出必然既少又慢,结果是吸收少,生物利用度差。但崩解度只是指药片崩裂为小于某号筛孔(一般为10号工业筛)所需的时间,并不考虑药物从这些小粒中溶出的速度如何。例如,有两种泼尼松片、崩解都只有2分半钟,但溶出标示量一半所需时间相差很大,一种仅4.3min,而另一种则长达173min。抗糖尿病药甲苯磺丁脲片也有类似的崩解好但溶出速度很慢的情况发生。以上两例中溶出速度慢的药片,其疗效都不及溶出速度快的那种。影响片剂生物利用度的剂型因素很多,除晶形、粒度等已提及的因素外,崩解剂、滑润剂、稀释剂等辅料的品种、用量都有影响。此外,压片压力大小对药物的溶出速度也有一定影响。
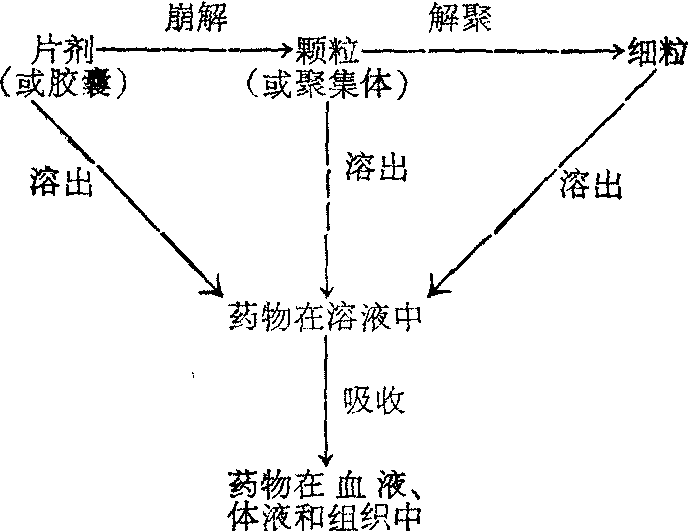
图3药物从片剂中的崩解、解聚集和溶出的图解
包衣片 根据包衣种类的不同,包衣片中药物溶出速度可以有很大参差。糖衣、薄膜衣溶解较快,影响不大,肠溶衣如所用包衣材料不当或用量过多,可能在整个肠道都不溶解。即使所包的肠溶衣材料及用量都符合要求,由于单个药片在胃中的停留时间从1.5~5.75小时不等,对于每4~6小时给药一片的情况,有时可能造成第一个药片还未越过幽门而第二个药片又接踵而至,这样两个剂量就同时进入十二指肠,以致接受了双倍剂量。如将肠溶衣片改为包肠溶衣的颗粒剂,可避免上述双倍剂量的危险。小肠空腹时颗粒每分钟移动约1cm。故从幽门到回盲瓣约需4~5小时。药物在小肠中停留时间的长短,与其生物利用度可能有密切关系。
口服剂型的生物利用度还与生理状态如胃的蠕动、空腹与否、食物种类等生理因素有关。
除口服给药剂型外,肌内注射给药、吸入给药如气雾剂、肛管给药剂型如栓剂等也与疗效有密切关系。一般认为肌内注射吸收较口服剂型为快且完全,但以混悬注射剂或乳状液注射剂作肌内注射时,吸收有时不及口服迅速; 某些用丙二醇及乙醇等溶剂溶解的药物作肌内注射时,例如苯妥因注射剂、安定注射剂、地高辛注射剂,肌注后溶剂扩散,药物沉淀在注射部位,故其临床疗效较口服为差。气雾剂因其雾粒可深抵肺泡,后者总面积约在25~100m2,故药物很快被吸收并发生药效,如复方异丙肾上腺素气雾剂。
- 唱反调是什么意思
- 唱口是什么意思
- 唱口声是什么意思
- 唱古文是什么意思
- 唱句子是什么意思
- 唱叫是什么意思
- 唱叫扬疾是什么意思
- 唱号儿是什么意思
- 唱吉利是什么意思
- 唱同调是什么意思
- 唱名是什么意思
- 唱名投票是什么意思
- 唱名法是什么意思
- 唱名表决是什么意思
- 唱吟是什么意思
- 唱吼是什么意思
- 唱呀儿哟是什么意思
- 唱呀呼嗨儿是什么意思
- 唱呀咦儿呦是什么意思
- 唱呻是什么意思
- 唱呼是什么意思
- 唱呾是什么意思
- 唱和是什么意思
- 唱和和神是什么意思
- 唱和的诗是什么意思
- 唱和,应答是什么意思
- 唱哈是什么意思
- 唱哈利是什么意思
- 唱哈节是什么意思
- 唱哈节为什么祭镇海大王是什么意思
- 唱响是什么意思
- 唱响子是什么意思
- 唱响社会主义文化的主旋律是什么意思
- 唱哩罗、招来牧竖,相尔汝、取次沙鸥。是什么意思
- 唱唐宣是什么意思
- 唱唤是什么意思
- 唱唱儿是什么意思
- 唱唱咧咧是什么意思
- 唱唱歌歌是什么意思
- 唱唱的是什么意思
- 唱唱舞舞是什么意思
- 唱善是什么意思
- 唱善若出一口是什么意思
- 唱喏是什么意思
- 唱喝是什么意思
- 唱喝百道是什么意思
- 唱嚎是什么意思
- 唱四值功曹是什么意思
- 唱坐腔是什么意思
- 唱大仙的是什么意思
- 唱大戏是什么意思
- 唱大江东是什么意思
- 唱大黑的是什么意思
- 唱大鼓的吃石灰——白说是什么意思
- 唱天是什么意思
- 唱头是什么意思
- 唱头奶是什么意思
- 唱头牌是什么意思
- 唱女儿是什么意思
- 唱好是什么意思