理想气体lixiang qiti
从宏观上看,能服从状态方程pV=nRT的气体,称理想气体。从微观考察,有个“理想气体模型”,即指分子间除碰撞接触的瞬间外无作用力,分子本身的体积比其气体所占的空间可忽略不计。宏观状态方程是微观模型的体现,即pV=nRT实际是不考虑分子间的作用力及其分子本身的体积。显然,理想气体状态方程对真实气体是不适用的。真实气体的情况较复杂,不同的真实气体可有不同的状态方程。不论符合什么样状态方程的真实气体,若真实气体的压力趋近于零,意味着气体有效空间接近于无穷大,此时,分子间距离很远,分子间的作用力及分子本身的体积均可忽略不计。因此,“零压”时,服从任一状态方程的真实气体,均可视为理想气体。如果对结果要求不是十分精确的,通常压力为101325 Pa,不论何种气体也可直接应用理想气体状态方程去求解。
从热力学看,凡是能严格遵循下列3条规律的气体,均可称为理想气体。
❶服从理想气体状态方程;
❷符合焦耳定律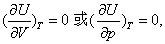 说明理想气体的内能只是温度的函数,与其压力或体积无关;
说明理想气体的内能只是温度的函数,与其压力或体积无关;
❸摩尔等压热容Cpm与摩尔等容热
容CV,m之差值恒定; 即Cpm-Cv,m=R(通用气体常数) 。这3条关键是第一条,故一般常用物态方程定义理想气体。
现实中并不存在什么理想气体,但为何要有这一定义呢?因理想气体能集中概括真实气体的共性。如果把理想气体比做一般,真实气体犹如个性,实为是一般与个别的关系。先熟悉一般,后探讨个别,是符合认识论规律的。
理想气体lixiang qiti
对实际气体的性质加以简化而提出的理想模型。从宏观角度看,理想气体在所有情况下都具有下述两个性质:
❶服从物态方程pV=γRT,式中p、V、γ分别为气体的压强、体积、摩尔数;R为普适气体常量;T为用理想气体温标量度的温度。
❷服从焦耳定律U=U(T),即理想气体的内能仅是温度的函数,与压强或体积无关。从微观角度看,理想气体分子的体积与分子间距离相比是可以忽略不计的,除弹性碰撞外,分子之间、分子与器壁之间没有相互作用。
引入理想气体这一理想模型的意义有二:
❶提出理想模型是科学研究的方法。不同的气体或同一气体处于不同状态时,遵从理想气体物态方程的准确程度是不同的,但在压强趋于零的极限情况下,各种气体都严格遵循上述方程。这说明各种气体具有共性。理想气体正是突出气体的共性,忽略其次要因素而提出的理想模型。掌握了理想气体的规律就便于进一步研究真实气体。
❷现实意义。在温度不太低和压强不太高的条件下,可以把真实气体视为理想气体。在通常条件下,真实气体往往可以作为理想气体来处理。例如:对于氮气等较难液化的气体,在0℃下只要压强不高于107帕,用理想气体物态方程计算的结果,误差一般都小于1%;对于二氧化碳等较容易液化的气体,在室温下,当压强为105帕时,用理想气体物态方程计算的结果误差一般约为2%~3%。内燃机中的燃气也可视为理想气体。真实气体的温度越高、压强越低,它的性质就越接近于理想气体。
理想气体
又称“完全气体”。理论上假想的一种把实际气体性质加以简化的气体,即指从宏观上说严格遵循玻意耳定律等规律,从微观角度来看分子本身的体积和分子间的作用力都可以忽略的气体。许多实际气体(如氢、氧等)在通常温度和压强下的行为接近理想气体。
理想气体
见“物理”中的“理想气体”。
理想气体
ideal gas
理想气体
ideal gas
- 中国古今作家真名笔名笔名真名便检是什么意思
- 中国古今名人大辞典是什么意思
- 中国古今名联鉴赏是什么意思
- 中国古今名胜遗迹长联是什么意思
- 中国古今地名大辞典是什么意思
- 中国古今地名对照表是什么意思
- 中国古今姓氏辞典是什么意思
- 中国古今实用对联大全是什么意思
- 中国古今工具书大辞典是什么意思
- 中国古今巧对妙联大观是什么意思
- 中国古今教育家是什么意思
- 中国古今称谓全书是什么意思
- 中国古今给日本取的各种别号是什么意思
- 中国古代、近代文学是什么意思
- 中国古代两大工程是什么意思
- 中国古代个性心理学思想是什么意思
- 中国古代中央官学是什么意思
- 中国古代九大名关是什么意思
- 中国古代书法家是什么意思
- 中国古代书法家辞典是什么意思
- 中国古代书画图目是什么意思
- 中国古代书画图目(一)是什么意思
- 中国古代书画目录是什么意思
- 中国古代书籍史是什么意思
- 中国古代书籍史话是什么意思
- 中国古代书院是什么意思
- 中国古代书院制度是什么意思
- 中国古代交通是什么意思
- 中国古代人口思想是什么意思
- 中国古代人文名篇鉴赏辞典是什么意思
- 中国古代传说是什么意思
- 中国古代体操是什么意思
- 中国古代体育是什么意思
- 中国古代作家名言荟萃是什么意思
- 中国古代信用是什么意思
- 中国古代信用与信用机构是什么意思
- 中国古代信用机构是什么意思
- 中国古代六大经济改革家是什么意思
- 中国古代兵制是什么意思
- 中国古代兵器是什么意思
- 中国古代兵器图是什么意思
- 中国古代兵器图说是什么意思
- 中国古代兵器图集是什么意思
- 中国古代兵法精粹类编是什么意思
- 中国古代兵法精萃类编是什么意思
- 中国古代养生学派是什么意思
- 中国古代养生家与养生著作是什么意思
- 中国古代养生术百种是什么意思
- 中国古代养生长寿论是什么意思
- 中国古代军事大辞典是什么意思
- 中国古代军事大辞典︱凡例是什么意思
- 中国古代军事大辞典︱前言是什么意思
- 中国古代军事大辞典︱编委名单是什么意思
- 中国古代军事学奠基人是什么意思
- 中国古代军事家列传是什么意思
- 中国古代军事思想是什么意思
- 中国古代军事文化大辞典是什么意思
- 中国古代农业是什么意思
- 中国古代农业害虫防治史是什么意思
- 中国古代农业技术简史是什么意思