高氯酸
高氯酸gaolusuan
化学式 HClO4,结构式

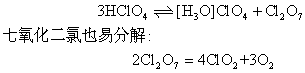
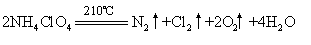
☚ 氯酸 溴 ☛
高氯酸
perchloric acid
- 混会儿是什么意思
- 混作是什么意思
- 混作一谈是什么意思
- 混作制是什么意思
- 混俏是什么意思
- 混俗和光是什么意思
- 混俗颐生录是什么意思
- 混儿是什么意思
- 混元是什么意思
- 混元三教九流石刻线画是什么意思
- 混元丹是什么意思
- 混元二十四式太极拳是什么意思
- 混元体是什么意思
- 混元初生太极是什么意思
- 混元史前是什么意思
- 混元史前时代是什么意思
- 混元圣纪是什么意思
- 混元子母大枪是什么意思
- 混元掌是什么意思
- 混元教是什么意思
- 混元散是什么意思
- 混元桩是什么意思
- 混元母是什么意思
- 混元气是什么意思
- 混元生是什么意思
- 混元盒是什么意思
- 混元盒五毒全传是什么意思
- 混元膏是什么意思
- 混元音是什么意思
- 混充是什么意思
- 混充人形儿是什么意思
- 混充人样是什么意思
- 混充八代是什么意思
- 混充其间是什么意思
- 混充大个儿牲口是什么意思
- 混充大人灯是什么意思
- 混充大力丸是什么意思
- 混充大料豆是什么意思
- 混充大牲口是什么意思
- 混充高雅是什么意思
- 混先是什么意思
- 混光照明设计手册是什么意思
- 混入内部的腐蚀者、破坏者是什么意思
- 混入内部的腐蚀者﹑破坏者是什么意思
- 混入沙土等异物是什么意思
- 混六是什么意思
- 混养是什么意思
- 混冒是什么意思
- 混军赚城是什么意思
- 混军赚将是什么意思
- 混冥是什么意思
- 混凝是什么意思
- 混凝剂是什么意思
- 混凝土是什么意思
- 混凝土与钢铁的大师是什么意思
- 混凝土体积稳定性和抗裂性理论与技术是什么意思
- 混凝土侧压力是什么意思
- 混凝土养护是什么意思
- 混凝土冬期施工手册是什么意思
- 混凝土减水剂是什么意思