金属与酸之间的置换反应
金属与酸之间的置换反应jinshu yu suan zhijian dezhihuan fanying
反应的实质是金属原子与酸电离出的氢离子之间的氧化-还原反应,产物是氢气和盐。常见反应:
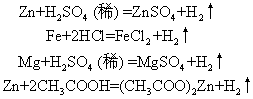
这类反应的规律:
❶金属越活泼越易与酸反应,如,钾、钠等活泼的金属与酸反应十分剧烈,常伴随轻微的爆炸。
❷参加反应的酸必须是可溶性的非氧化性酸,溶液中氢离子浓度越大,反应越易进行。酸的强弱和浓度都对反应有很大影响。例如,锌与浓盐酸反应比与稀盐酸反应剧烈,锌与同浓度的盐酸和醋酸反应时,前者剧烈得多。氧化性酸 (浓硫酸、浓硝酸、稀硝酸等) 与金属反应时,氢离子不得电子,不属于置换反应。
❸反应后生成的盐难溶时,会复盖在金属表面,使金属与酸脱离接触,反应难以进行。例如,铅与硫酸反应时,生成难溶的硫酸铅,反应发生后立即停止。如果反应后生成的盐完全水解,金属与酸也不能反应。例如,铝与氢硫酸不反应,因硫化铝在水中完全水解时生成氢硫酸。
❹升高温度可使反应速度加快。例如,铁与稀硫酸在常温下反应很微弱,加热后,反应则十分剧烈。
此外,当金属中含有较不活泼的金属杂质时,会发生原电池反应,使反应速度加快。例如,与同浓度的酸反应时,粗锌比纯锌剧烈得多。
☚ 金属与水的反应 金属与盐溶液间的置换反应 ☛
- 次广泛、广泛子宫切除术是什么意思
- 次张汉公言怀(1)是什么意思
- 次施彦执韵(1)是什么意思
- 次氯酸钙漂液是什么意思
- 次氯酸钠是什么意思
- 次氯酸钠是什么意思
- 次氯酸钠是什么意思
- 次氯酸钠是什么意思
- 次氯酸钠是什么意思
- 次氯酸钠漂液是什么意思
- 次氯酸钠的分析是什么意思
- 次甲氯地孕酮是什么意思
- 次石湖书扇韵(1)是什么意思
- 次萧冰崖梅花韵(1)是什么意思
- 次要作用是什么意思
- 次要的模具零件是什么意思
- 次韵东坡还自岭南是什么意思
- 次韵傅惟肖(1)是什么意思
- 次韵和景彝省闱宿斋二首(1)(其二)是什么意思
- 次韵天锡提举(1)是什么意思
- 次韵子由题平山堂(1)是什么意思
- 次韵子瞻以红带寄王宣义(1)是什么意思
- 次韵子瞻登望海楼五绝(选一)(1)是什么意思
- 次韵子瞻题郭熙画秋山(1)是什么意思
- 次韵孔宪蓬莱阁(1)是什么意思
- 次韵方夏日五首。时渠在禹溪,余乃居福严(其三)(1)是什么意思
- 次韵李节推九日登南山(1)是什么意思
- 次韵柳通叟寄王文通是什么意思
- 次韵王荆公题西太一宫壁二首(1)是什么意思
- 次韵秦少游春江秋野图二首(1)是什么意思
- 次韵黄斌老所画横竹(1)是什么意思
- 欧·亨利(O. Henry, 1862—1910)是什么意思
- 欧也妮·葛朗台是什么意思
- 欧仁·苏(Eugne Sue, 1804—1857)是什么意思
- 欧仑施雷厄(Adam Gottlob Oehlenschlger,1779—1850)是什么意思
- 欧共体1962年农产进口关税立法是什么意思
- 欧共体1995年农产进口关税立法是什么意思
- 欧共体共同农业基金立法是什么意思
- 欧共体农业价格政策立法是什么意思
- 欧共体农产价格政策立法是什么意思
- 欧共体农产出口信贷政策立法是什么意思
- 欧共体农产出口补贴政策立法是什么意思
- 欧共体农产干预价格立法是什么意思
- 欧共体农产目标价格立法是什么意思
- 欧共体农产绿色汇率立法是什么意思
- 欧共体农产货币补偿立法是什么意思
- 欧共体农产贸易普惠制立法是什么意思
- 欧共体农产进口卫生标准立法是什么意思
- 欧共体农产进口原产地规则立法是什么意思
- 欧共体农产进口技术规则立法是什么意思
- 欧共体大气污染控制立法是什么意思
- 欧共体废弃物处理立法是什么意思
- 欧共体振动噪声控制立法是什么意思
- 欧共体植物贸易检疫立法是什么意思
- 欧共体欧洲野生动物保护立法是什么意思
- 欧共体气体粉尘控制立法是什么意思
- 欧共体水质污染控制立法是什么意思
- 欧共体海洋污染控制立法是什么意思
- 欧共体濒危动植物贸易控制立法是什么意思
- 欧共体环境保护任务立法是什么意思