量子效率quantum efficiency,photosynthesis
又称量子产额。光合过程中每吸收一个光量子所能还原的CO2分子数或释放氧的分子数。即以量子为基础的光合效率。按光化学当量定律,1个光量子最多引起1个分子(或电子)的变化,所以量子效率的最高值不可能大于1。用活力高的植物材料,在CO2还原不是限制因子的条件下,测得光合作用的量子效率为0.08~0. 12。
量子效率
量子效率liangzi xiaolu
光化学反应一般包含若干个基元步骤。把一个反应物分子吸收1个光子而活化的基元步骤称为光化学反应的初级过程。在初级过程中,1个光子活化1个反应物分子。把活化微粒所进行的一系列基元步骤,称做光化学反应的次级过程。例如HI在光作用下分解
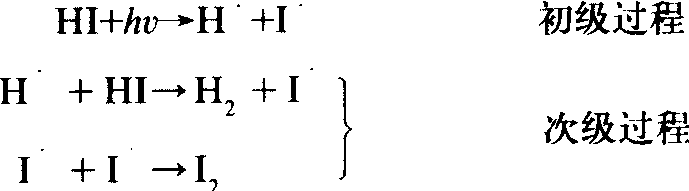
1个分子吸收1个光子在进行光化学反应之前,有时会自动发射出光子而失活,或经分子内部能量的传递或无辐射的跃迁而失活。有时分子吸收1个光子而产生自由基或某种催化剂,从而引起链反应或催化反应。因此吸收1个光子不一定就使1个分子发生光化学反应,有失活次级过程存在时,发生光化学反应的分子数可能小于吸收的光子数; 因吸收光子而发生链或催化反应时,则反应分子数大于吸收的光子数。因此定义: 吸收1个光子所能引起反应的微粒数,称量子效率,用表示,则

1 mol光子称为1爱因斯坦。量子效率是对整个过程而言的,包括初级过程和次级过程在内。它可以小于1,等于1和大于1(见下表)。
某些气相光化学反应的量子效率
| 反 应 | λ/(nm) | 量子效率 | 备注 |
| 2NH3=N2+3H2 SO2+Cl2=SO2Cl2 | 210 420 | 0.25 1 | 随压力而变 |
| 2HI=H2+I2 | 207~282 | 2 | 在较高的温度、 压力范围内保持 常数 |
| 2HBr=H2+Br2 | 207~253 | 2 | |
| H2+Br2=2HBr | 600以下 | 2 | 在近200℃(25 ℃时极小) |
| 3O2=2O3 | 170~253 | 1~3 | 近于室温 |
| CO+Cl2=COCl2 | 400~436 | 约103 | 随温度而降,与 反应物压力也有 关 |
| H2+Cl2=2HCl | 400~436 | 高达106 | 随pH2及杂质而 变 |
☚ 光化学反应 感光反应 ☛
量子效率
又称“量子产量”。每吸收1光量子能同化的二氧化碳或释放的氧气分子数。通常用量子需要量的倒数来表示。活力最高的植物材料在暗反应不起限制作用的条件下,所得到的光合放氧的最低量子需要量为8—12,相当于0.12—0.08的量子效率。
- 削竹拳是什么意思
- 削竹箭是什么意思
- 削笔是什么意思
- 削籍是什么意思
- 削籍为民是什么意思
- 削约是什么意思
- 削老是什么意思
- 削职是什么意思
- 削职为民是什么意思
- 削职罢是什么意思
- 削肉是什么意思
- 削肩是什么意思
- 削肩弧足空首布是什么意思
- 削肩细腰是什么意思
- 削肩膀是什么意思
- 削肿是什么意思
- 削背是什么意思
- 削苗是什么意思
- 削草是什么意思
- 削草不除根,萌芽依旧发是什么意思
- 削草除根是什么意思
- 削菘是什么意思
- 削菜是什么意思
- 削落是什么意思
- 削葱是什么意思
- 削藩是什么意思
- 削藩策是什么意思
- 削衣是什么意思
- 削衣贬食是什么意思
- 削角是什么意思
- 削觚为圆是什么意思
- 削觚庐是什么意思
- 削说论是什么意思
- 削足而适履,杀头而便冠。是什么意思
- 削足适履是什么意思
- 削足适屦是什么意思
- 削趾适履是什么意思
- 削趾适屦是什么意思
- 削蹄是什么意思
- 削蹄刀是什么意思
- 削迹是什么意思
- 削迹捐势是什么意思
- 削铁是什么意思
- 削铁如泥是什么意思
- 削铁如泥,吹毛即断是什么意思
- 削铁无声是什么意思
- 削除是什么意思
- 削除军籍是什么意思
- 削除平定是什么意思
- 削除瓦解是什么意思
- 削除,铲除是什么意思
- 削青是什么意思
- 削面落皮是什么意思
- 削鞘是什么意思
- 削鞭是什么意思
- 削骨淡去是什么意思
- 削骨脸是什么意思
- 削,切是什么意思
- 削𢴈𢴈是什么意思
- 剋是什么意思