腺垂体的激素
腺垂体由腺体细胞组成,至少分泌七种激素。按它们的化学性质可分为三大类:
❶肽类激素,包括促肾上腺皮质激素(ACTH),促黑色细胞激素(MSH)与脂肪酸释放激素(LPH);
❷糖蛋白激素,包括黄体生成素(LH)、卵泡刺激素(FSH)与促甲状腺素(TSH);
❸蛋白激素,包括生长素、催乳素及促黄体激素(某些动物)。
促肾上腺皮质激素 是最早从腺垂体中提纯并确定化学结构的一种激素。它是含39个氨基酸的开链多肽,分子量为4,567。用化学方法断裂分子的实验证明,1~20的氨基酸(N端)是生物学活性所依赖的基团,其余氨基酸是与免疫有关的基团,也可能对激素的运输与防止分子的破坏有一定关系。从不同动物所得的ACTH,其1~23的氨基酸排列顺序相同。ACTH分子中4~10的氨基酸序列与αMSH分子中4~10的氨基酸序列相同,所以也具有一定的促黑色细胞激素的作用。ACTH的生理功能主要是促进肾上腺皮质的功能,它与肾上腺皮质中特异性受体结合后,通过cAMP的作用,使胆固醇易于进入线粒体内,并转化为孕烯醇酮,加强糖皮质激素的生物合成,从而增加糖皮质激素的分泌与释放。据测定,人垂体约含ACTH 250μg,一般情况下,每日约消耗10μg,其储量可供大约一月之用。在应激状态,分泌可增加10倍。另外,ACTH还可刺激RNA的合成,从而产生新的肾上腺皮质蛋白,促进细胞分化与增生,使肾上腺重量增加。所以,加强糖皮质激素的生物合成和促进皮质束状带的增生是ACTH的两大生理作用。ACTH对醛固酮的合成影响很小。切除垂体后,血中皮质醇的浓度立即下降,补充ACTH可使其迅速回升;由于正常情况下,肾上腺皮质激素对垂体促肾上腺皮质功能存在负反馈抑制作用,当肾上腺皮质功能不足时,血中ACTH增加,反之,有所减少。ACTH的分泌表现昼夜周期性节律,清晨最高(6~8点),夜间最低(18~23点)。ACTH在血液中的半衰期较短,为25分钟,肾脏可能是破坏ACTH的场所之一。
在特殊实验条件下,ACTH除作用于肾上腺外,还对肾上腺以外的组织产生各种作用,如,促进脂肪细胞中脂肪水解,刺激垂体释放生长素等,近来还证明,ACTH存在于脑组织,与脑啡肽的分布大体一致。
促黑色细胞激素 人的MSH主要由垂体促肾上腺细胞分泌,部分由垂体后叶产生。MSH有α与β两种,结构上与ACTH相似,具有促进黑色素合成及增强黑色素沉着的作用。
腺垂体还分泌一种含91个氨基酸的多肽,具有促进脂肪酸释放的作用,称为β-LPH; 其41~58片段与β-MSH的结构相同,故也有促黑色细胞的作用。近年来发现,β-LPH的其他片段,61~76,61~77,61~91,可出现于脑组织,与脑组织的吗啡受体结合,从而产生镇痛作用。这几个片段分别称为α、γ与β-内啡肽。在应激状态下,β-内啡肽可能与ACTH一起从垂体释放出来,前者起镇痛作用,后者起“抗炎”作用。
促性腺激素 腺垂体分泌的FSH与LH,能促进性腺的活动;此外,胎盘还分泌一种促进性腺活动的激素,绒毛膜促性腺激素CG。这三种激素与TSH的化学结构相似,都是由α与β两条肽链通过糖基连结而成,三种激素的α链相似。α链没有生物活性,β链活性也弱,二者合在一起就产生生物活性。β链起决定作用。
男人和女人腺垂体分泌的FSH与LH在结构上没有差别,但其生理作用不同。
卵巢 人卵巢约含二百万个卵原细胞。每个卵泡在卵泡膜内层细胞出现以前,其生长发育不受促性腺激素的控制。卵泡由卵巢皮质转移至髓质后出现卵泡膜内层细胞,这时由于髓质血液比较丰富,卵泡才开始受血液中激素的调控,在FSH与LH的影响下不断发育生长。LH的作用之一是与内层细胞上的LH受体结合,使内层细胞分泌雄激素(睾酮与雄甾烷二醇),并合成少量17β-雌二醇。FSH则与卵泡内颗粒细胞上的FSH受体结合,激活颗粒细胞的芳香化酶,使内层细胞分泌的雄激素转变为11-β雌二醇。血中雌二醇的浓度逐渐增高,其结果是:一方面进一步增强LH与FSH与相应受体结合的能力,促进卵泡继续生长发育,卵泡腔逐渐增大,泡液增多;另一方面,雌二醇又将作用于下丘脑与腺垂体,使FSH的分泌受到抑制,血中FSH浓度下降(负反馈),但此时LH浓度基本维持不变。由于卵泡液有蓄积FSH与雌二醇的作用,在血中FSH与雌二醇浓度处于低水平时,生长中的卵泡仍可受到FSH与雌二醇的持续刺激而继续长大,颗粒细胞将充分发育生长,膜上LH受体也增多,并在LH作用下获得制造孕酮的能力。而那些发育迟缓尚无泡腔的卵泡,缺乏卵泡液,没有储存FSH与雌二醇的可能,所以,在血中FSH浓度降低时,由于FSH不足,雄激素无法转变为17-β雌二醇,以致卵泡内雄激素愈积愈多,而雌二醇缺乏或过少,结果成为闭锁卵泡,停止发育。
在卵泡发育生长时期,在血中促性腺激素的浓度变化不大的情况下,血中雌二醇也表现逐渐升高,这是卵巢本身周期性分泌的特征。接近排卵时,雌二醇的浓度可达200~400pg/ml,持续36小时后,血中LH浓度将出现一次高峰(猴,其他动物的具体数字不同),这一高峰称为LH峰。LH峰产生的机理,虽不完全清楚,一般认为与雌二醇有关。雌二醇可能刺激腺垂体合成LH,提高腺垂体对促性腺素释放激素(GnRH)的反应性,还可能促使下丘脑释放较多的GnRH;这些作用均可使血中LH大量增加。
LH峰出现引起的几项重大的变化:
❶卵泡合成激素的方式由产生雄激素与雌二醇转变为合成孕酮,这是因为高浓度LH抑制了芳香化酶而且阻止LH与内层细胞上LH受体结合;
❷LH加强蛋白水解酶对卵泡壁的破坏作用,导致卵泡破裂,发生排卵;
❸LH促进卵巢合成前列腺素(PG)E与F,PGE和PGF也有引起卵泡破裂的作用;
❹LH使颗粒细胞发生形态变化,成为黄体细胞。如卵子没有受精,人的卵巢可产生PG2α,使黄体萎缩和“溶解”,重新开始另一月经周期。如果怀孕,则由胎盘产生人绒毛膜促性腺激素(hCG),hCG具有促黄体作用,可维持黄体存在。
睾丸 FSH刺激睾丸精细管,促进精子的形成与成熟过程,而LH则刺激其间质细胞合成和分泌睾(甾)酮。所以,LH又称为促间质细胞激素(ICSH)。人睾丸可能产生一种物质,叫做“抑制素”(inhibin),对FSH的分泌具有抑制作用,作用地点是垂体,但也不能排除作用于下丘脑的可能性。
垂体内FSH与LH的量,9岁左右才开始出现,过早出现是病态,但也不能迟于13岁,随着年龄增长而有所增加,有月经的人,垂体FSH量为200IU左右,LH量在700IU上下。卵巢功能不全者,血中FSH增加。FSH与LH在血浆中的浓度为10-11mol/L,半衰期为30~60分钟。36%的FSH可排入尿中,仅5%的LH在尿中出现,其余部分的代谢过程,迄今不明。
促甲状腺激素 它的化学结构虽已基本阐明,尚无高度纯品,分子量为28,000。TSH对甲状腺有多方面的作用。切除垂体或垂体功能不全时,甲状腺发生萎缩,功能低下,补充适量TSH可纠正这种变化。在TSH的作用下,甲状腺增大,血流增加。如注射TSH或将TSH加入甲状腺的培养液里,几分钟之内,即可见到甲状腺上皮细胞顶端伸出伪足吞饮腺泡内胶质,发生入胞作用,并由溶酶体释放水解酶将胶粒中的甲状球蛋白予以水解,使T3和T4释放入血。这是TSH的主要生理作用。此外,TSH对甲状腺逆浓度梯度摄碘、甲状球蛋白合成、T3与T4的合成等过程也有促进作用。上述各种作用主要通过cAMP系统,也可能有前列腺素参与。
TSH通过磷酸戊糖通路及葡萄糖氧化过程可大大提高耗氧量,增进葡萄糖氧化以增强能量供应。在葡萄糖供应不足时,甚至可动用内源能量的物质,例如磷脂代谢的加强,有机磷酸化物的分解;另一方面,RNA的合成也有所加强,说明在TSH影响下,分解代谢与合成代谢均增强,前者为后者提供能量,有利于甲状腺激素的合成。
TSH还可作用于非甲状腺组织,促进脂肪组织的水解过程。
垂体含TSH的量很小,估计只有4IU(1~2ng/ml)左右。血浆中浓度在10-10mol/L上下,半衰期为50分钟,在甲状腺功能低落时,半衰期延长,功能亢进时缩短。肾脏是破坏TSH的主要器官。据计算,每天由垂体释放的TSH约为165mIU。
催乳素 催乳素 (PRL) 是垂体分泌的一种蛋白质激素,与垂体的生长素(GH)及胎盘产生的绒毛膜生长激素(hCS)的结构相似,催乳素含198个氨基酸,具有二硫键。
催乳素的主要生理作用是发动和维持泌乳。实验证明,乳腺腺管的生长发育有赖雌激素、生长素及肾上腺皮质激素的协同作用,而腺泡小叶的发育与增生则需要孕激素与催乳素。怀孕期,虽然乳腺具有泌乳的潜力,但由于血液中存在高浓度的雌激素与孕激素,它们对垂体催乳作用产生反馈抑制,另外,孕酮也有抑制乳腺合成乳糖和乳蛋白的作用,不能发生泌乳; 产后,由于胎盘排出,雌激素与孕激素浓度大大降低,反馈抑制取消,才开始泌乳,但是需在催乳素、胰岛素及皮质激素存在的条件下,泌乳功能才能维持,不致中断。哺乳时,吸吮乳头的动作,可通过神经反射通路,将吸吮引起的冲动传达到下丘脑,下丘脑存在分泌催乳素释放因子(PRF)的肽类神经元,在接到传来的冲动后,即释放PRF,与此同时,分泌催乳素释放抑制因子(PIF)的神经元受到抑制而停止工作,这样,PRF与PIF两种肽类神经元的密切协调,便使垂体发生反射性的催乳素分泌,血中浓度增加。在人类,哺乳开始后的半小时,血中催乳素浓度出现一次高峰,为下一次喂乳作好准备。动物切断乳腺神经,或是将脊髓或脑干毁损后以上泌乳反射消失。
泌乳与排乳有所区别。排乳是由催产素引起的,催产素使乳腺的肌上皮细胞收缩,将乳汁挤压到乳池,然后排放出来。
催乳素可作用于下丘脑而抑制GnRH的释放,从而减少FSH与LH的分泌,故哺乳期中母亲月经暂时停止。
人垂体中PRL含量较GH为少,约含100μg。血浆中浓度正常妇女为9.0±0.6ng/ml,男子为6.2±0.6ng/ml。半衰期大致是20~30min,与GH半衰期接近。男子的催乳素作用不明。
生长素 生长素GH是垂体分泌的另一蛋白质激素。不同动物生长素的化学结构、生物活性与免疫活性差异很大。人生长素hGH由191个氨基酸组成,具有两个二硫基,结构与人催乳素相近,因此,生长素有弱PRL作用,PRL有弱GH作用,二者在免疫上也有交叉;有人用水解酶处理hGH,发现分子被破坏50%以后,仍然具有生物活性,强度不减,因此认为在肽链中大约有100个氨基酸是生物活性的中心。动物的生长素制剂对人无效。GH的生理作用如下:
(1) 促进生长: 生长是机体的新组织按生理规律的增加,是一个很复杂的过程,生长素只是起重要作用的一种因素,但过少或过多均将严重影响正常生长。人幼年时期缺少hGH将患侏儒症,hGH过盛,发生“巨人症”,成年后骨骺发育成熟,长骨不再生长,此时如hGH分泌过多,身长不再增加,短骨却可过度长大,出现肢端肥大症,内脏如肝、肾等也将增大,产生内脏肥大现象。临床经验证明,hGH的测定对以上疾病的诊断很有帮助,同时也说明垂体hGH分泌的增加或减少与以上病症有关。可是,也需指出,体液中hGH的浓度有时并不反映生长的情况。胎儿及婴儿时期身体增长最快,hGH的分泌,并无明显平行关系; 成长中儿童与已停止生长的成人,血液hGH浓度基本一致; 又如,肾上腺、性腺、甲状腺、子宫及其他附性器官的增长,都是明显的组织增加,都不依赖hGH。hGH有促进软骨形成与钙化的作用。去垂体后,软骨停止发育,长骨骺板萎缩变窄; 补充hGH又能使软骨重新增长,骺板增宽血清磷酸酯酶活性相应增高,说明成骨作用加强。在hGH持续作用下,长骨继续增长,骺板融合与骨成熟过程延迟; 其他激素如性激素和甲状腺激素也有促进骨生成的作用,但同时加速骺板融合与骨成熟过程,作用不完全一样; 此外胰岛素在成骨过程中可起一定的“允许作用”。
hGH在促进软骨生长的同时,还能促进结缔组织、皮肤以及肝肾等内脏器官发生相应性增长。关于GH对软骨组织的作用机理,离体软骨实验发现: GH加入去垂体动物的软骨培养液中不能使软骨恢复生长,而加入正常动物血浆却有效,去垂体动物的血浆无效,说明GH对软骨生长并无直接作用,而是通过血液中某种因子间接地发挥作用。进一步的研究证明,GH可使肝脏,也许还有肾和肌肉产生一种因子,称为生长介质(SM),促进35SO2-4、3H-胸苷、3H-尿苷及14C-亮氨酸等进入软骨组织,增加其中胶原组织、硫酸软骨素以及核酸与蛋白质的形成,从而使软骨细胞分裂,基质增殖,软骨生长。由于SM主要有促硫酸化作用,所以,又称为“硫酸化因子”。胰岛素与丰富营养有利于此因子的形成,相反,慢性肝病,雌激素及肾上腺皮质激素可能抑制其形成。SM除对软骨有作用外,对肌肉与纤维母细胞等也有类似作用。
(2) GH对代谢的影响: GH对中间代谢与能量代谢均有广泛的影响。GH促进蛋白质合成,增强钙、钠、钾及磷等元素的储留,同时,通过抑制糖的消耗,加速脂肪分解,使能量来源由糖代谢转向脂肪代谢,有利于机体的生长与修复过程。有人认为:GH的作用是使机体各组织的组成维持“年青”状态,蛋白质与体液较多而脂肪较少。
❶蛋白质代谢: 在GH的影响下,氨基酸进入细胞的速度增加,尿氮减少,机体出现正氮平衡,与此同时,钠与钾随之也进入细胞,参与细胞新生,硫、钙、磷等元素则进入骨,提供骨生长的原料; 但是,氨基酸进入细胞,不是细胞蛋白质合成增加的主要原因,因为将GH注射入去垂体动物后,分析肌肉内氨基酸含量结果未发现有较大增加; 却发现肝脏组织中核蛋白体、mRNA及tRNA等明显减少,RNA合成受到抑制,如补充GH,则上述现象立即得到纠正。因此,人们认为GH促进蛋白质合成的作用主要是促进RNA的合成。
❷糖代谢:GH对糖代谢的影响,主要有生糖作用与糖原稳定作用两个方面。生糖作用的主要表现是:降低肌肉与脂肪组织对葡萄糖的摄取与利用以及促进肝脏产生葡萄糖,结果是对抗胰岛素的作用。去垂体动物血糖降低,对胰岛素过敏与此有关。所以,GH的生糖作用又称为抗胰岛素作用。糖尿病人,如摘除垂体,在注射hGH后立刻看到病情加重,酮症增加,清楚说明GH具有生糖作用。关于GH的糖原稳定作用: 在去垂体动物处于饥饿状态时,表现明显,此时动物心肌与骨胳肌肉的糖原迅速消失; 而正常动物饥饿时,骨胳肌保持糖原不变,心肌糖原还略有增加。总之,GH减少葡萄糖的消耗,增加糖原的储备。有人认为长期使用GH可导致垂体性糖尿病。
❸脂肪代谢: GH可增加脂肪的转移,加强分解,从而使脂肪组织的脂肪量减少。在人,特别是肢体中脂肪减少,血中游离脂肪酸增加。游离脂肪酸进入肝脏后在肝内氧化以提供能量,酮体生成增多,机体的呼吸商有所降低。游离脂肪酸增加有抑制葡萄糖氧化的作用,有时称为“葡萄糖-脂肪代谢环”。在生理情况下,hGH不是促进体内脂肪分解的唯一主要因素。
垂体含GH相当丰富,可达垂体干重4~8%(人),每个腺体约含3~5mg,不同年龄的含量相同。GH分泌表现明显的昼夜节律,正常成人血浆GH约为1~5ng/ml,饭后3~4小时略有升高; 睡眠影响较大,深睡一小时后明显升高,可达40ng/ml,持续2~3小时,有人认为此时GH增加可能对机体的同化过程及修复功能有利。体力活动、饥饿和情绪紧张等均可使GH有所增加。GH使能量的来源由糖代谢向脂代谢转移,以燃烧脂肪来应付葡萄糖之不足,对以上情况可能非常有利。年老人血中GH浓度与成年人相近,而且,在应激状态下,分泌GH的能力与成年人相比,并无逊色。这进一步说明GH的作用不仅限于促进生长。
GH的半衰期为20~25min,其降解与排泄情况,不甚了解。
- 尿合是什么意思
- 尿后余沥是什么意思
- 尿吓是什么意思
- 尿含铁血黄素检查是什么意思
- 尿吮是什么意思
- 尿哈是什么意思
- 尿哩高是什么意思
- 尿嘧啶是什么意思
- 尿嘧啶氮芥是什么意思
- 尿嚎嚎是什么意思
- 尿囊是什么意思
- 尿囊憩室是什么意思
- 尿囊液是什么意思
- 尿囊素是什么意思
- 尿囊腔接种是什么意思
- 尿囊酸是什么意思
- 尿圈[t
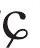 y
y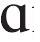
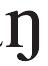 ]是什么意思
]是什么意思 - 尿坑泥是什么意思
- 尿培养是什么意思
- 尿埾是什么意思
- 尿堂是什么意思
- 尿塔是什么意思
- 尿壑是什么意思
- 尿壶是什么意思
- 尿壶包是什么意思
- 尿壶滓是什么意思
- 尿外渗是什么意思
- 尿多是什么意思
- 尿大圆上皮细胞是什么意思
- 尿失禁是什么意思
- 尿失禁分度是什么意思
- 尿失禁病人的护理是什么意思
- 尿孔是什么意思
- 尿小圆上皮细胞是什么意思
- 尿小尿是什么意思
- 尿少是什么意思
- 尿尿是什么意思
- 尿尿[suei]是什么意思
- 尿尿去了屙下屎来——连稀稠都拿不住了是什么意思
- 尿尿把把是什么意思
- 尿屎袋是什么意思
- 尿屎齐流是什么意思
- 尿崩亭是什么意思
- 尿崩停是什么意思
- 尿崩症是什么意思
- 尿崩症护理是什么意思
- 尿巴子是什么意思
- 尿巷子是什么意思
- 尿布是什么意思
- 尿布垫是什么意思
- 尿布大王是什么意思
- 尿布皮炎是什么意思
- 尿布红斑是什么意思
- 尿布银屑病是什么意思
- 尿帕是什么意思
- 尿常规化验是什么意思
- 尿常规检查是什么意思
- 尿床是什么意思
- 尿床儓是什么意思
- 尿底高是什么意思