肝脏毒理学
肝脏毒理学主要研究外源性毒物与肝脏的相互作用,探讨影响肝脏毒作用的各种因素,阐明中毒性肝损害的特点和作用机理,为防治中毒性肝病提供理论依据。
肝脏具有肝动脉和门静脉双重血液供应,又有肝静脉和胆道两条输出通路。化学物不论是通过胃肠道吸收经门静脉进入肝脏或来自体循环,都可在肝脏内贮留和转化。肝小叶的血液循环由外周流向中央区,故血液中若含有毒物时,首先接触到毒物的是肝小叶外周带的肝细胞,而缺氧时则对中央静脉附近的肝细胞影响较大。进入肝脏的毒物及其代谢产物,可通过血液循环经肾脏排出,或随胆汁直接流入肠道而排出体外。有些毒物或其代谢产物进入肠道后又可被肠壁重吸收,经门静脉返回肝脏,形成肠肝循环。
很多化学物能引起肝细胞的亚细胞结构改变,影响其正常功能。肝细胞中线粒体、粗面及滑面内质网、游离核蛋白体和多核蛋白体等,与肝细胞的能量供应,蛋白质、糖原和脂类的合成和代谢以及外源性化学物的转化有密切关系。对化学物转化具有重要意义的肝微粒体混合功能氧化酶主要存在于滑面内质网,其中最重要的是细胞色素P-450和NADPH-细胞色素P-450还原酶。线粒体和胞液中也含有参与生物转化的酶系,如胺氧化酶、醇脱氢酶等。不同部位的肝细胞功能有所不同,如肝小叶外周带呼吸酶活性较高,细胞分裂和再生能力较强; 而中央区特别富有微粒体酶,对化学物的转化能力较大。化学物对肝脏的损害程度和表现与其作用部位有关。肝脏内有各种各样的酶。在正常情况下,肝脏酶主要分布于肝细胞内,而在血清中其活性很低。肝细胞损伤时由于细胞膜通透性增高,或因组织坏死,细胞破裂,可使大量酶释放到血液中,故测定血清中这些酶的活性对判断肝损害具有一定意义。
凡能引起肝损害的化学物,通称为肝脏毒物。有些毒物对肝脏具有特殊亲和力或特异性作用,这类毒物称为亲肝性毒物。肝脏毒物的种类很多,主要有:
❶脂肪族卤代烃类(四氯化碳、氯仿、三氯乙烯、四氯乙烷等)。
❷卤代环烃类(氯萘、溴苯等)。
❸某些金属、类金属(磷、砷、硒、锑等)。
❹其他化合物如二甲基亚硝胺、甲酸烯丙酯、二甲胺基偶氮苯等。
❺天然毒素(鹅膏蕈碱、黄曲霉毒素等)。许多药物如氯丙嗪、巴比妥酸、磺胺、异烟肼、丙咪嗪、四环素、保泰松、氟烷、蛋白同化类固醇、雌激素等,在一定条件下也可能引起肝损害,称为药物性肝损害。
肝脏是外源性化学物进行生物转化的主要器官,亲肝性毒物都是在肝脏进行生物转化的。经生物转化后,大部分毒物的毒性降低或消失,但也有一部分毒物的毒性反而增强(参见“生化毒理学”)。例如,四氯化碳引起肝损害,主要由于它在肝微粒体酶系催化下产生的代谢产物的毒作用所致。烯丙醇和甲酸烯丙酯引起肝坏死,是由于醇脱氢酶使其转化为活性很强的代谢产物丙烯醛所致。有些化学物经体内转化后生成强烷化剂、芳基化剂或酰化剂而引起肝损害。但同一物质在不同条件下可表现为解毒或增毒。例如,溴苯引起坏死可能是由于其代谢产物环氧溴苯对肝细胞的直接作用,但少量溴苯进入体内时,环氧溴苯可通过与谷胱甘肽共价结合而转化为硫醚氨酸经肾脏排出,故不致造成肝损害; 而大剂量时由于谷胱甘肽被耗竭,环氧溴苯与细胞内蛋白质、核酸等亲电子性大分子共价结合,则可导致细胞坏死。
关于肝脏毒物与其他化学物的联合作用问题,一般认为脂肪族醇类(甲醇、乙醇、异丙醇、丁醇等)能增强卤代烃类的肝毒性。这种增毒作用可能是在微粒体酶系内相互作用的结果。肝微粒体酶系的活性与年龄、性别、营养及健康状况等因素有关,并可被许多物质诱导或抑制。凡经生物转化后毒性消失或减弱的毒物,酶诱导剂可增强其解毒作用。反之,如代谢产物的毒性大于原化合物时,则其毒作用强度与代谢功能活性大小成正比。例如,酶诱导剂苯巴比妥能刺激肝微粒体混合功能氧化酶活性,使细胞色素P-450及有关的酶浓度增高,加速化合物的代谢,因而能使这类化学物的毒作用增强。有些化学物如多环芳香烃3-甲基胆蒽、苯并(a)芘及有机氯杀虫剂DDT、六六六、氯丹等也有类似作用。相反,酶抑制剂SKF-525A能抑制细胞色素P-450,减慢肝血流及外源性物质的吸收,故能防止毒性代谢产物对肝脏的损害。还有许多化学物也能防止或减少卤代烃对肝脏的损害,但其保护作用机理不一。二硫化碳能拮抗大剂量四氯化碳对动物的致死作用,与它能引起内质网脂质变性,破坏细胞色素P-450,从而阻止四氯化碳转化为毒性代谢产物有关。硫代氨基甲酸酯类能减轻四氯化碳引起脂肪变性的作用,可能与四氯化碳的代谢酶被抑制有关。
很多毒物在一定条件下能引起中毒性肝损害,但不同的肝脏毒物,所引起的损害类型可有不同。
肝脏毒物按其作用机理可分为固有肝脏毒物和主要取决于个体特异体质的毒物两大类。固有肝脏毒物对肝脏的损害是由于毒物本身的毒作用所致,主要表现为坏死、脂肪变性、肝内胆汁郁积、肝纤维化等。这类毒物引起肝损害的共同特征是:
❶发生率高,在一定剂量作用下多数人都可发生,其形态改变通常具有某些相对特异性。
❷肝损害程度与剂量大小有一定的关系。
❸潜伏期较恒定,一般较短。
❹肝损害模型能在实验动物中复制。
主要取决于个体特异体质的毒物所致肝损害的共同特征是:
❶发生率低,仅见于少数人,其形态改变为非特异性的,多伴有免疫反应现象。
❷大多数没有明显的剂量依存关系。
❸潜伏期长短不一,有的很短,有的可长达数周乃至数月。
❹肝损害模型不能在动物身上复制。多数引起肝损害的药物属于这一类,其毒性一般不大,组织学上主要表现为胆汁郁积和/或肝细胞损害(炎症反应),常伴有发热、皮疹、关节痛及血液和组织中嗜酸性粒细胞增多。有时仅见肝功能障碍而无黄疸或其他体征。再次接触同类药物往往引起复发。
中毒性肝损害随着作用方式的不同,可有多种的分类方法。急性中毒性肝损害按其形态改变特征可分为肝细胞损害型、肝内胆汁郁积型和混合型 (见表)。肝细胞损害又可分为坏死和脂肪变性两类; 胆汁郁积有的属单纯型(无炎症反应),有的伴有胆管周炎。肝细胞脂肪变性和坏死可以分别单独存在,也可以同时或先后出现。例如,四氯化碳、氯仿、黄磷、二甲基亚硝胺、二甲胺基偶氮苯等,不但能引起肝细胞脂肪变性,而且多伴有坏死。坏死有时仅累及少数肝细胞(局灶性坏死),较重者形成带状坏死,一般为肝小叶中央区坏死。严重损害时整个肝小叶细胞坏死(大块坏死)或发生急性黄色肝萎缩。肝脏组织再生能力强,多有可能恢复,除非整个肝小叶被破坏,但也可能形成纤维化,甚至导致肝硬变。
急性中毒性肝损害类型
| 类型 | 形态改变主要特征 | 临床上相 似的肝病 | 病死率 |
| 肝细胞损 害 | |||
| 坏死 | 肝细胞变性、坏死。线粒体肿 胀、变形、溶解。滑面内质网肥 大、增生;粗面内质网断裂、扩 张,出现空泡,多核蛋白体解 聚、消失 | 病毒性 肝炎 | 10~50% |
| 脂肪变 性 | 肝细胞脂肪浸润,内质网内可 见甘油三酯堆积,形成微脂粒 (liposome) | 妊娠脂 肪肝 | 较高 |
| 胆汁郁积 | |||
| 无炎症 | 毛细胆管、肝细胞内胆汁郁 积,无炎症反应。毛细胆管扩张, 微绒毛减少、消失。肝细胞内质 网肥大,有时出现空泡 | 阻塞性 黄疸 | <1% |
| 伴有炎 症 | 胆汁郁积伴有胆管周炎,常见 嗜酸性粒细胞浸润 | 阻塞性 黄疸 | <1% |
| 混合型 | 既有肝细胞损害,又有胆汁郁 积 | 非典型 病毒性肝 炎或阻塞 性黄疸 | 视病情 轻重而定 |
肝脏毒物长期作用可引起慢性肝炎、肝纤维化、肝硬变或肿瘤。例如,二甲基亚硝胺、黄曲霉毒素B1急性作用引起肝细胞脂肪变性和坏死,慢性损害可导致癌变。氯乙烯可引起肝血管肉瘤。多次给予亚致死量四氯化碳可使动物产生肝硬变。甲基多巴、异烟肼、磺胺类药物有时可引起慢性肝炎和肝硬变。吩噻嗪类药物可引起慢性胆汁郁积,还可能伴有进行性肝纤维化。慢性酒精中毒可导致慢性坏死和增生过程而造成肝硬变。
多数肝脏毒物如黄磷、砷、鞣酸等达到一定剂量时即可直接损伤肝细胞膜和内质网等亚微结构,特别是影响线粒体功能,引起肝细胞代谢紊乱,最后导致细胞死亡。肝细胞脂肪变性主要由于脂蛋白合成障碍而影响肝细胞内脂类的运出所致。有些毒物如砷、氨基甲酸乙酯(乌拉坦)能损伤血管,使其通透性增高,引起出血或血栓。毒物引起的特异性反应常与变态反应和遗传因素有关,如药物性肝炎和胆汁郁积可视为迟发型细胞免疫反应的一种表现。化学物引起的慢性肝炎往往具有一些免疫学特征,血清中γ球蛋白增多与组织学改变有一定的相关。免疫反应可能是肝损害的一个重要因素,但这种反应是不是肝损害的原发性原因尚难肯定。
中毒性肝损害的机理主要从下列几方面进行了研究,其中有些问题还有待进一步探讨。
(1) 脂肪变性: 许多化学物能引起大量脂肪 (主要是甘油三酯) 堆积于肝实质细胞内。一般认为甘油三酯分泌障碍是形成脂肪肝的主要因素,而甘油三酯分泌障碍又与脂蛋白合成抑制密切相关。
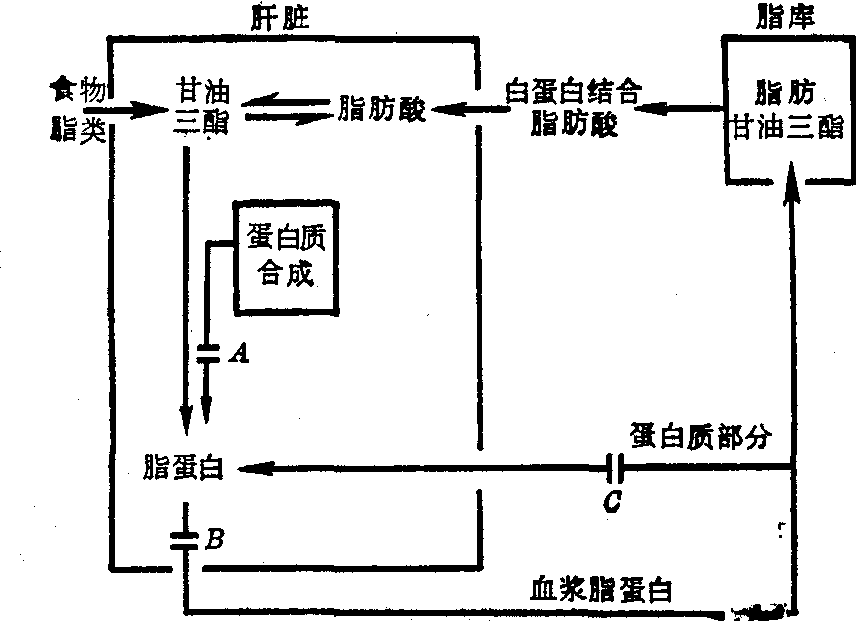
脂肪循环示意图
A: 四氯化碳和乙硫氨酸可能阻断脂蛋白的合成。
B: 乙硫氨酸还可能阻滞脂蛋白的转运。C: 乳清酸可能阻滞蛋白质的再利用,致使甘油三酯不能与载脂蛋白结合。
在正常情况下,肝脏甘油三酯以脂蛋白方式释放到血液中。很多化学物(四氯化碳、黄磷、乙硫氨酸、嘌呤霉素、乳清酸等)能干扰脂蛋白的合成和转运,致使甘油三酯堆积于肝细胞内(见图)。这时血浆中脂类和脂蛋白含量减少,特别是对运输甘油三酯起主要作用的极低密度脂蛋白含量显著下降,其下降程度与肝细胞内甘油三酯堆积量呈平行关系。
甘油三酯合成过多可能也是引起脂肪肝的一个因素。甘油三酯合成速度与底物(脂肪酸和甘油磷酸酯)浓度成正比。例如,胼中毒时,由于脂解作用加强,游离脂肪酸从脂库中逸出,血浆中脂肪酸含量增高,可使肝细胞内甘油三酯合成增多而引起脂肪堆积。
肝细胞脂肪变性可导致肝细胞死亡,但脂肪肝不一定都伴有坏死。例如,乙硫氨酸、甲酸烯丙酯、嘌呤霉素、放线菌酮能引起脂肪肝,而没有或仅有少量坏死。异丙嗪能防止四氯化碳引起肝细胞坏死,却不能防止脂肪肝。
(2) 蛋白质合成抑制: 肝脏蛋白质合成抑制是中毒性肝损害常见的一种早期表现。光学显微镜检查可见肝细胞坏死前胞浆内嗜碱性物质消失。电子显微镜检查发现胞浆出现空泡,内质网变形,膜界限不清,核蛋白体颗粒消失。许多肝脏毒物对信息核糖核酸(mRNA)的合成有显著影响,并可使其分解破坏,因而造成蛋白质合成障碍。但蛋白质合成障碍不一定导致坏死和脂肪变性。例如,乙硫氨酸、放线菌酮能抑制蛋白质合成,但不引起坏死。硫代乙酰胺能抑制蛋白质合成,却不引起脂肪变性。放线菌素D能抑制蛋白质合成,但既不引起坏死,也不引起脂肪堆积。相反,肼中毒时出现坏死和脂肪变性,而蛋白质合成并未受影响。因此,蛋白质合成抑制可能不是中毒性肝损害的原发性病变。
(3) 脂质过氧化反应: 脂质过氧化反应是中毒性肝损害的一种特殊表现形式。例如,四氯化碳在肝微粒体NADPH-细胞色素P-450还原酶和细胞色素P-450催化下产生一种氧化能力很强的代谢中间产物,可引起肝细胞结构和功能改变,破坏膜的磷脂,导致肝细胞脂肪变性和坏死。四氯化碳的C—Cl键在体内易断裂而产生具有毒作用的自由基——三氯甲基 (·CCl3)。两个·CCl3自由基还可能缩合为CCl3—CCl3。CCl4释出的自由基首先侵犯内质网膜脂质部分,与其中不饱和脂肪酸支链双键结合,生成过氧化物; 而过氧化脂质又可释出自由基,侵袭另一些脂质,形成一种破坏性的自身催化连锁反应。这种破坏作用不断扩大,造成内质网、线粒体等的形态和功能改变,最后导致细胞坏死。脂质过氧化反应能抑制肝微粒体酶和葡糖-6-磷酸酯酶活性,阻滞蛋白质合成,影响肝细胞产生和排出低密度脂蛋白的能力,致使脂肪不能运出而堆积于细胞内。因此,脂质过氧化反应可能是造成肝细胞坏死和脂肪堆积的一个原因。抗氧化剂和自由基清除剂吩噻嗪类、维生素E、二苯基对苯二胺,没食子酸丙酯及一些巯基化合物(如半胱胺)能消除或减轻四氯化碳对肝脏的毒作用,这种解毒作用也支持了上述假说。碘仿及其他一些卤代烃类都有过氧化作用,但不同化合物的作用有很大差异。一般说来,这种作用与键解离能成反比。例如,三氯溴甲烷键解离能低,很易断裂,其自由基反应活性很高,而氯仿则相反,过氧化作用很弱。目前已知许多肝脏毒物能引起脂质过氧化反应,但这种作用究竟是不是肝损害的原发性原因,尚不能确定。
(4) 胆汁郁积反应: 有一些化学物如α-异硫氰酸萘酯(ANIT)、牛磺石胆酸、2-乙基-2-苯基丁酰胺,能在不同种属动物中引起肝内胆汁郁积。ANIT一次口服可引起大鼠胆汁郁积和血胆红素过多。胆汁郁积的机理尚不太清楚,可能与下列情况有关:
❶肝细胞功能改变,羟化酶活性降低,使羟基化合物石胆酸等过剩。
❷肝细胞膜和微绒毛受损,引起排泄功能障碍,胆汁酸在肝细胞内堆积,并在毛细胆管内形成胆栓。
❸细胞膜通透性改变,水、电解质及胆汁盐和其他溶质的重吸收增多,致使毛细胆管内胆汁浓缩沉积,形成胆栓。肝细胞功能改变和毛细胆管阻塞又可相互影响,形成恶性循环,从而加剧胆汁郁积。
中毒性肝病的防治要点是: 凡患有肝病或对肝脏有不良影响,能促进肝损害的疾病 (如糖尿病、甲状腺机能亢进等)和嗜酒、营养不良、体弱多病者以及怀孕期、哺乳期、更年期妇女,不宜从事接触肝脏毒物的作业。
许多药物可能引起肝损害,使用时应注意观察患者反应和病情变化; 凡对该药物有过敏史者,应避免使用或根据情况慎用。
发现有肝损害或其他禁忌证时,应即停止接触和使用该毒物(药物),给予适当治疗,并与病毒性肝炎等传染病患者严格隔离,防止感染。
积极治疗引起肝损害的原发病以及并发病和继发病,及时采用特殊解毒、排毒剂和护肝药物,避免用药过多,禁用可能对肝脏有不良影响的药物如氯丙嗪、磺胺等。
中毒性肝病与病毒性肝炎往往不易鉴别,应根据详细接触史、现场调查、临床观察、化验检查等方面综合资料全面分析。目前尚缺乏可靠的特异性鉴别诊断指标,特别是慢性中毒时发病缓慢,诊断较难,且不能排除两种肝病同时并存的可能性。
- 张英(4)是什么意思
- 张英伦是什么意思
- 张英华是什么意思
- 张英奎是什么意思
- 张英才是什么意思
- 张英明是什么意思
- 张英杰是什么意思
- 张英洪是什么意思
- 张英渤是什么意思
- 张英超是什么意思
- 张英辉是什么意思
- 张英阁是什么意思
- 张英风是什么意思
- 张英麟是什么意思
- 张茂是什么意思
- 张茂之是什么意思
- 张茂先是什么意思
- 张茂先集是什么意思
- 张茂和是什么意思
- 张茂和称病被贬案是什么意思
- 张茂妻陆氏的人物故事|评价|小传,张茂妻陆氏的事迹|史鉴是什么意思
- 张茂宗是什么意思
- 张茂实是什么意思
- 张茂嶂是什么意思
- 张茂度是什么意思
- 张茂德是什么意思
- 张茂忠是什么意思
- 张茂昭是什么意思
- 张茂材是什么意思
- 张茂松是什么意思
- 张茂清是什么意思
- 张茂炯是什么意思
- 张茂珍是什么意思
- 张茂镛是什么意思
- 张范是什么意思
- 张范1是什么意思
- 张范2是什么意思
- 张范与贼寇是什么意思
- 张范村是什么意思
- 张范通梦是什么意思
- 张范风流是什么意思
- 张茜是什么意思
- 张茜茜是什么意思
- 张茵是什么意思
- 张荃是什么意思
- 张荃翁是什么意思
- 张荆州画赞是什么意思
- 张荆野是什么意思
- 张草是什么意思
- 张荐是什么意思
- 张荐明是什么意思
- 张荣是什么意思
- 张荣仁是什么意思
- 张荣发是什么意思
- 张荣培是什么意思
- 张荣奎是什么意思
- 张荣宪是什么意思
- 张荣庆是什么意思
- 张荣晋是什么意思
- 张荣森是什么意思