米氏方程MichaelisMenten equation
酶促反应中反应速度与底物浓度间相互关系的动力学函数表达式。即v=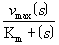 ,其中v为反应速度;vmax为反应最大速度;〔s〕为底物浓度;Km为米氏常数。是酶促反应动力学中的基本公式。在酶浓度和其它条件不变的情况下,当底物浓度较低时,酶促反应速度与底物浓度呈正比,表现为一级反应;当底物浓度很大时,反应速度不再随底物浓度增加而增加,表现为零级反应;当底物处于中间浓度时,表现为混合级反应。米凯利斯(L. Michaelis)和门顿(M.L.Menten)从酶与底物先形成酶底物中间复合物的假说出发,首先推导得此方程,故称之米氏方程。后来,布利格斯(G.E.Briggs)和哈丹尼(J.B.S.Haldane)根据酶底物中间复合物浓度在反应的一段时间内不变(稳态或恒态)的前提下,对此方程作了一些补充和发展。
,其中v为反应速度;vmax为反应最大速度;〔s〕为底物浓度;Km为米氏常数。是酶促反应动力学中的基本公式。在酶浓度和其它条件不变的情况下,当底物浓度较低时,酶促反应速度与底物浓度呈正比,表现为一级反应;当底物浓度很大时,反应速度不再随底物浓度增加而增加,表现为零级反应;当底物处于中间浓度时,表现为混合级反应。米凯利斯(L. Michaelis)和门顿(M.L.Menten)从酶与底物先形成酶底物中间复合物的假说出发,首先推导得此方程,故称之米氏方程。后来,布利格斯(G.E.Briggs)和哈丹尼(J.B.S.Haldane)根据酶底物中间复合物浓度在反应的一段时间内不变(稳态或恒态)的前提下,对此方程作了一些补充和发展。
米氏方程
表明底物浓度与酶促反应速度间定量关系的公式。从下列假定出发,即1.酶,底物与酶-底物复合物间迅速达成平衡;2.反应速度为起始速度,与酶-底物复合物的浓度成正比,以致从产物逆转成酶-底物复合物的反应可略去不计。可用公式明确表示v=V[S]/(Km+[S]),式中v为反应的起始速度,V为最大速度,[S]为底物浓度,Km为底物常数,也称米氏常数。
米氏方程
早在19世纪,虽然人们尚未了解酶的化学本质,但通过酶的动力学的研究,观察pH、温度、底物浓度、抑制剂和激活剂对于酶促反应速度的影响,获得了不少关于酶催化反应机制的知识。
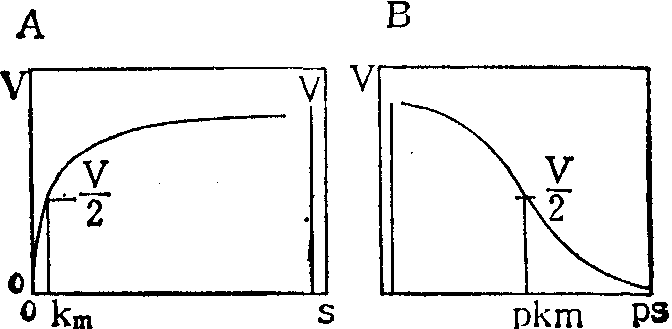
酶催化反应速度与底物浓度的关系
(A)为反应速度V对底物浓度S作图;(B)为V对ps(-logs)作图。
与非催化的反应相比,酶催化反应速度与底物浓度的关系不呈线性而是双曲线形关系,即随着底物浓度的提高,酶促反应速度会达到一个最大值(图)。1913年德国生化学家Michaelis和Menten提出了著名的米氏方程
- 员馀庆是什么意思
- 员首是什么意思
- 呙是什么意思
- 呙堕髻是什么意思
- 呙宋台遗址是什么意思
- 呙斜是什么意思
- 呚是什么意思
- 呛是什么意思
- 呛㞗哩是什么意思
- 呛三十是什么意思
- 呛不吃顺不吃是什么意思
- 呛个满脸是什么意思
- 呛了棒子是什么意思
- 呛人是什么意思
- 呛住是什么意思
- 呛儿是什么意思
- 呛农是什么意思
- 呛劲是什么意思
- 呛劲儿是什么意思
- 呛呛是什么意思
- 呛呛儿是什么意思
- 呛呛哺哺是什么意思
- 呛咕是什么意思
- 呛咕呛咕是什么意思
- 呛咳是什么意思
- 呛哼是什么意思
- 呛喀是什么意思
- 呛喉风是什么意思
- 呛嗽是什么意思
- 呛场是什么意思
- 呛子是什么意思
- 呛实是什么意思
- 呛得筛是什么意思
- 呛棒子是什么意思
- 呛棒子货是什么意思
- 呛死是什么意思
- 呛死人是什么意思
- 呛水是什么意思
- 呛汤是什么意思
- 呛火是什么意思
- 呛炭是什么意思
- 呛爆鲜词是什么意思
- 呛白是什么意思
- 呛眉黑眼是什么意思
- 呛菜是什么意思
- 呛面儿是什么意思
- 呛面风是什么意思
- 呛风是什么意思
- 呛风冷气是什么意思
- 呛食哑喉是什么意思
- 呛食喉风是什么意思
- 呛食风是什么意思
- 呛饭是什么意思
- 呛鼻是什么意思
- 呜是什么意思
- 呜
.jpg) 是什么意思
是什么意思 - 呜乎哀哉是什么意思
- 呜儿是什么意思
- 呜儿喊叫是什么意思
- 呜叫是什么意思