离子反应
离子反应lizi fanying
指有离子参加的化学反应。反应物中有电解质且电离出自由离子时才可能发生离子反应。离子反应大多数在水溶液中进行,少数离子化合物在熔融状态也可发生离子反应。固态物质与电解质的浓溶液反应时,则应根据反应原理确定是否属于离子反应。例如,浓硫酸中存在大量硫酸分子和少量的氢离子,硫酸根离子。它与铜反应时,硫酸分子表现出强氧化性,该反应不属于离子反应; 它与固体亚硫酸钠反应时,氢离子和亚硫酸根离子结合成亚硫酸 (不稳定,分解为二氧化硫和水) ,该反应属于离子反应。
溶液中的离子反应可分为:
❶离子交换型的复分解反应,包括生成沉淀、气体、弱电解质3类。例如:
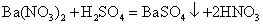
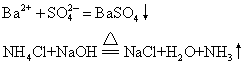
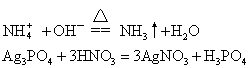
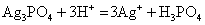
❷氧化-还原类型的离子反应,包括置换反应和较复杂的氧化-还原反应。例如:
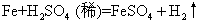
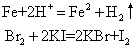
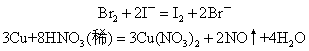
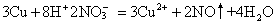
❸盐类的水解反应。例如:
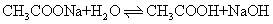
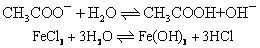
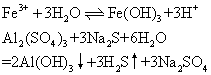
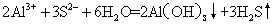
❹有配合物参加或生成的反应。例如:
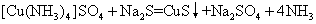
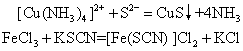
Fe3++SCN-=[Fe(SCN)]2+
❺电极反应,包括原电池反应和电解反应两类。例如,在铜、锌、稀硫酸组成的原电池中:
负极(Zn):Zn-2e=Zn2+
正极(Cu):2H++2e=H2↑
用石墨作电极电解硫酸铜溶液时:
阴极: 2Cu2++4e=2Cu
阳极:4OH--4e=2H2O+O2↑
此外,根据参加反应的微粒,离子反应可分为离子与离子、离子与原子、离子与分子3类。例如:
Cu2++2OH-=CuOH2↓
2Fe3++Cu=2Fe2++Cu2+
2Br-+Cl2=Br2+2Cl-
☚ 酸式盐溶液的酸碱性 溶液中离子大量共存的条件 ☛
离子反应
ionic reaction
- 路由选择是什么意思
- 路界线是什么意思
- 路畔是什么意思
- 路畔的蔷薇是什么意思
- 路畔蔷薇是什么意思
- 路登是什么意思
- 路登云是什么意思
- 路的一端是什么意思
- 路的中间是什么意思
- 路的交叉口是什么意思
- 路的各部是什么意思
- 路的尽头是什么意思
- 路的表面是什么意思
- 路监司是什么意思
- 路盲是什么意思
- 路石是什么意思
- 路矿大臣是什么意思
- 路碑是什么意思
- 路神是什么意思
- 路神 保一路平安是什么意思
- 路祭是什么意思
- 路福是什么意思
- 路秀峰是什么意思
- 路秉杰是什么意思
- 路程是什么意思
- 路程不远是什么意思
- 路程很远是什么意思
- 路程的距离是什么意思
- 路程较远的是什么意思
- 路程近的是什么意思
- 路程远是什么意思
- 路程,道路是什么意思
- 路税务提领是什么意思
- 路穷才是穷是什么意思
- 路穷流水远更远,目断夕阳西复西。是什么意思
- 路穷车绝是什么意思
- 路竭无君子是什么意思
- 路端电压是什么意思
- 路端电压(端电压)是什么意思
- 路符是什么意思
- 路節是什么意思
- 路粹是什么意思
- 路索雷姆手反射是什么意思
- 路纪是什么意思
- 路纸是什么意思
- 路线是什么意思
- 路线·政策是什么意思
- 路线不明是什么意思
- 路线价是什么意思
- 路线价区段是什么意思
- 路线价法是什么意思
- 路线价法的操作步骤是什么意思
- 路线价法的计算是什么意思
- 路线侦察是什么意思
- 路线勘测是什么意思
- 路线图是什么意思
- 路线导向设施是什么意思
- 路线指示牌是什么意思
- 路线教育是什么意思
- 路线斗争是什么意思