氮族元素
氮族元素danzuyuansu
位于周期表第VA族,包括氮N、磷P、砷As、锑Sb、铋Bi 5种元素,统称为氮族元素。从氮到铋依次由非金属—半金属—金属组成,是典型的主族元素,砷、锑、铋也称做砷分族。自然界的氮绝大部分以单质状态存在于空气中,磷均以化合物形态存在,最重要的是磷矿石,主要成分为Ca3(PO4)2。自然界的砷、锑、铋主要以硫化物矿存在,如雄黄As4S4,雌黄As2S3,辉锑矿Sb2S3,辉铋矿Bi2S3等。氮族元素的基本性质及其递变关系见表1。
表1 氮族元素的基本性质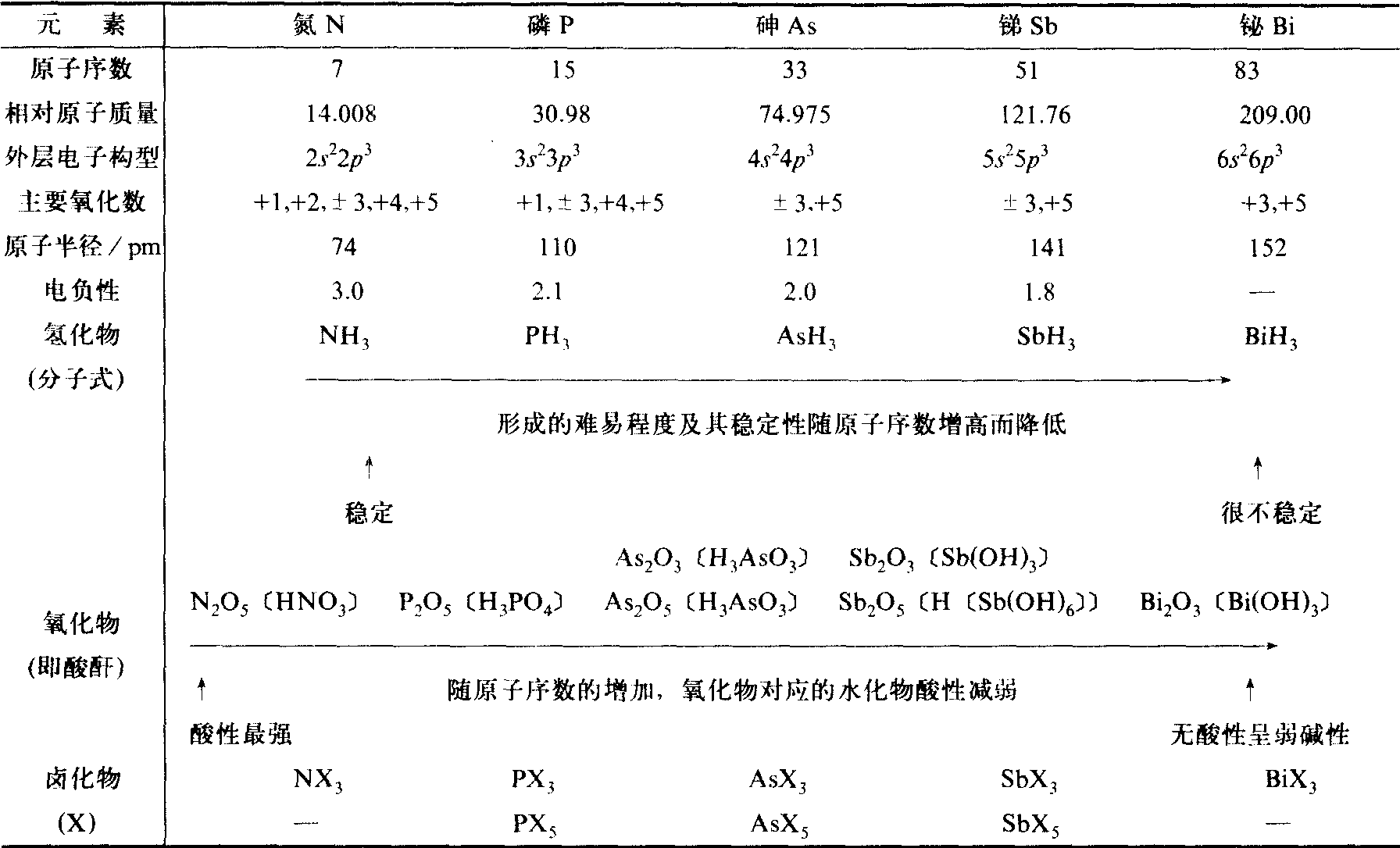
表2 氮族元素单质的物理性质
| 元 素 | 单质化学式 | 色 态 | 密度/g·cm-3 | 熔点/℃ | 沸点/℃ | 溶 解 性 |
| N P As | N2 P4 | 无色气体或液体 黑磷: 黑色固体 | 气1.2506(g·L-1) 2.7 | -209.86 | -195.8 | 不溶于CS2 |
| 红磷: 无定形粉末 | 2.34 | 590 | 200 | 溶于无水乙醇 | ||
| 紫磷: 单斜晶体 | 2.36 | 590 | ||||
| 白(黄)磷: 蜡状固体 | 1.82 | 44.1 | 280 | 溶于碱、 氨、 有机溶 剂 | ||
| As (灰) | 灰色金属光泽, 六方或 正交晶体 | 5.727 | 817 (28Pa) | 613 (升华) | 溶于HNO3 | |
| As (黑) | 黑色玻璃状, 无定形 | 4.73 | 270℃以上变灰砷 | |||
| As4 | 黄色固体, 立方晶体 | 2.026 | 358 (分解) | 溶于苯或CS2中 | ||
| Sb | Sb (灰) Sb (黄) | 银白色金属, 六方晶形 黄色透明固体 | 6.684 | 630.5 | 1750 | 溶于浓热H2SO4 极不稳定, 溶于CS2 |
| Sb (黑) | 黑色固体 | 5.3 | 不稳定, 微热转灰锑 | |||
| Bi | Bi | 银白色或微红色金属 | 9.80 | 271.3 | 1560±5 | 溶于热 H2SO4或 HNO3 |
氮和磷是生命的重要元素,分别占人体总质量的2.4%和0.9%。它们也是植物生长的重要营养元素,它们的化合物主要用做肥料。氮肥大多是氮的化合物,如硝酸钾、硝酸铵、氨水、碳铵等; 磷肥主要是无机磷酸盐。硝酸及其盐是制作炸药、染料和许多其他化工产品的重要原料。砷用做农药,锑、铋主要用于制作合金。氮族元素及其化合物在各方面都有着广泛的应用,在理论研究和国民经济中都有十分重要的意义。
☚ 醋酸铅 氮 ☛
- 春秋地名异文考是什么意思
- 春秋地名考略是什么意思
- 春秋地理考实是什么意思
- 春秋增注是什么意思
- 春秋备览是什么意思
- 春秋复始是什么意思
- 春秋夏正是什么意思
- 春秋外传国语注是什么意思
- 春秋大一统是什么意思
- 春秋大一统是什么意思
- 春秋大义是什么意思
- 春秋大义是什么意思
- 春秋大事表是什么意思
- 春秋大事表是什么意思
- 春秋大传补说是什么意思
- 春秋大全是什么意思
- 春秋女谱是什么意思
- 春秋孔义是什么意思
- 春秋存俟是什么意思
- 春秋宗朱辨义是什么意思
- 春秋家说是什么意思
- 春秋家说是什么意思
- 春秋尊孟是什么意思
- 春秋尊王发微是什么意思
- 春秋小学是什么意思
- 春秋属比考例是什么意思
- 春秋属辞是什么意思
- 春秋属辞会义残本是什么意思
- 春秋属辞比事记是什么意思
- 春秋属辞辨例编是什么意思
- 春秋岁星考是什么意思
- 春秋左传是什么意思
- 春秋左传事类年表是什么意思
- 春秋左传会要是什么意思
- 春秋左传函义是什么意思
- 春秋左传分国土地名是什么意思
- 春秋左传句解是什么意思
- 春秋左传地名考是什么意思
- 春秋左传学史稿是什么意思
- 春秋左传嵇氏音是什么意思
- 春秋左传服注存是什么意思
- 春秋左传杜注校勘记是什么意思
- 春秋左传杜注补辑是什么意思
- 春秋左传正义是什么意思
- 春秋左传正义是什么意思
- 春秋左传正义是什么意思
- 春秋左传注是什么意思
- 春秋左传注是什么意思
- 春秋左传注是什么意思
- 春秋左传王氏注是什么意思
- 春秋左传类对赋是什么意思
- 春秋左传类对赋注是什么意思
- 春秋左传类编是什么意思
- 春秋左传类解是什么意思
- 春秋左传补注是什么意思
- 春秋左传补疏是什么意思
- 春秋左传要义是什么意思
- 春秋左传诂是什么意思
- 春秋左传诂是什么意思
- 春秋左传识小录是什么意思