范德瓦耳斯方程
范德瓦耳斯方程fandewaersi fangcheng
真实气体物态方程的一种。1摩尔真实气体的范德瓦耳斯方程为:
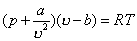
其中p、T分别是真实气体的压强和温度,v是真实气体的摩尔体积,a和b称为范德瓦耳斯修正量,是可由实验测得的常量,对不同的气体a、b的值不同,详见下表。质量为M,摩尔质量为μ的气体,范德瓦耳斯方程为:
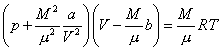
其中V是气体的体积。
范德瓦耳斯方程是考虑到气体分子的大小及分子间的相互作用力,对理想气体物态方程进行了两项修正而建立的,在建立范德瓦耳斯方程时使用了苏则朗(Sutherland)模型,即分子是有弱引力的刚球,1个摩尔的理想气体的物态方程为:pv=RT,p、T是理想气体的压强和温度,v是气体的体积,也就是分子自由活动的空间。
❶考虑到分子的大小所作的修正:由于分子有大小,从而使分子自由活动的空间减小为v-b。关于b的数值可以作如下的定性解释和估算,由于斥力的作用,一对分子接近到一定距离d时便不能再靠近,因此分子可以看作是一个直径为d的刚球,每一个分子周围都有4/3πd3的空间不允许另一个分子进入,即每一对分子都占有4/3πd3的空间,这个空间相当于分子固有大小(4/3πr3,r=d/2)的8倍,也就是说每个分子占有4倍固有体积的禁区,从而减小了分子自由活动的空间,因此修正量b=4NA(4/3πr3),NA是阿伏伽得罗常量,r是分子半径,b实际上是考虑到分子间的斥力所作的修正,修正后方程为p=RT/v-b。
❷考虑到分子间的引力所作的修正:分子在向器壁接近的过程中,在器壁附近由于受到气体内部分子的引力而减速,减小了分子与器壁碰撞时对器壁的冲量,从而压强较理想气体的压强减小了△p,真实气体的压强可表示为p=
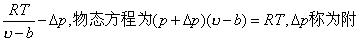 加压强,单位体积内的分子数n越大,单位时间内碰在器壁上的分子数越多,内部分子对飞向器壁分子的吸引力也越大,所以△p∝n2,或△p∝1/v2,写成△p=a/v2时,a是一个常量,最后得到1摩尔的范德瓦耳斯方程为(p+a/v2)(v-b)=RT。
加压强,单位体积内的分子数n越大,单位时间内碰在器壁上的分子数越多,内部分子对飞向器壁分子的吸引力也越大,所以△p∝n2,或△p∝1/v2,写成△p=a/v2时,a是一个常量,最后得到1摩尔的范德瓦耳斯方程为(p+a/v2)(v-b)=RT。范德瓦耳斯方程是真实气体物态方程中最简单,使用最方便,并有较明确物理意义的一个,它能给出高压下气体状态变化的关系(如左下表),它还可以指出气体存在临界点、气体在临界温度以下液化时的情况等。
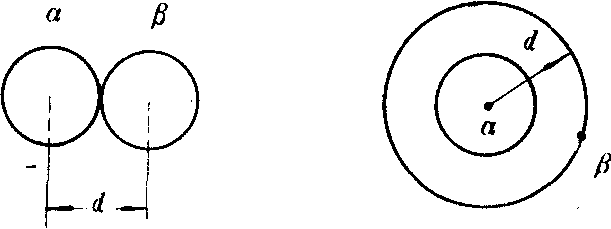
范德瓦耳斯常数a和b的实验值
| 气体 | a /1.013×10-1Pa·m6·mol-1 | b /10-3m3·mol-1 |
| 氩 | 1.345 | 0.03219 |
| 氯 | 6.493 | 0.05622 |
| 氦 | 0.03412 | 0.02370 |
| 氢 | 0.2444 | 0.02661 |
| 氖 | 0.2107 | 0.01709 |
| 氮 | 1.390 | 0.03913 |
| 氧 | 1.360 | 0.03183 |
| 水蒸气 | 5.464 | 0.03049 |
| 汞蒸气 | 8.093 | 0.01696 |
| 二氧化碳 | 3.592 | 0.04267 |
0℃时1摩尔氢在不同压强下的v、pv和
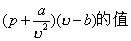
| ρ /105Pa | υ /10-3m3 | ρυ /102Pa·m3 | (ρ+a/υ2)(υ-b) /102Pa·m3 |
| 1 | 22.41 | 22.41 | 22.41 |
| 100 | 0.2241 | 22.41 | 22.41 |
| 500 | 0.06235 | 31.17 | 22.67 |
| 700 | 0.05325 | 37.27 | 22.65 |
| 900 | 0.04825 | 43.40 | 22.4 |
| 1000 | 0.0464 | 46.4 | 22.0 |
☚ 真实气体 普适气体常量 ☛
- 人的尸体是什么意思
- 人的属性是什么意思
- 人的希望是什么意思
- 人的平等是什么意思
- 人的度量宏远是什么意思
- 人的形体是什么意思
- 人的形体和内脏是什么意思
- 人的形状、模样是什么意思
- 人的德行成就是什么意思
- 人的心力是什么意思
- 人的志行品德是什么意思
- 人的态度、身份等突然改变是什么意思
- 人的态度作风是什么意思
- 人的思想言论是什么意思
- 人的思想随环境而变化是什么意思
- 人的思想,作风没有改变,一如既往是什么意思
- 人的性格、爱好各不相同或事物各有差异是什么意思
- 人的性格、行为不同一般是什么意思
- 人的总称是什么意思
- 人的意志,佛爷挫败不了是什么意思
- 人的意识是什么意思
- 人的意识、思维活动和一般心理状态是什么意思
- 人的感情是什么意思
- 人的感情亲密无间是什么意思
- 人的所作所为是什么意思
- 人的手指为什么长短不齐是什么意思
- 人的才情是什么意思
- 人的才能超出同辈是什么意思
- 人的担保是什么意思
- 人的教育是什么意思
- 人的整个身体和各种器官是什么意思
- 人的文学是什么意思
- 人的文学(节选)是什么意思
- 人的时令是什么意思
- 人的是非功过要到死后才能做出结论是什么意思
- 人的晚年是什么意思
- 人的晚年,暮年是什么意思
- 人的晚景美好是什么意思
- 人的智力构成是什么意思
- 人的智谋和力量可以战胜自然是什么意思
- 人的最珍贵的智力宝藏是什么意思
- 人的本事非凡,神通广大是什么意思
- 人的本性是什么意思
- 人的本性就是政治的动物是什么意思
- 人的本质是什么意思
- 人的本质对象化是什么意思
- 人的来历是什么意思
- 人的某种思想倾向是什么意思
- 人的榜样是什么意思
- 人的模拟是什么意思
- 人的欲望是什么意思
- 人的欲望不能太多、太高是什么意思
- 人的欲望嗜好是什么意思
- 人的欲望没有止境是什么意思
- 人的正确思想是从哪里来的是什么意思
- 人的正确思想是从哪里来的?是什么意思
- 人的气势是什么意思
- 人的气势宏大豪迈是什么意思
- 人的气度或文章等大气磅礴,豪放自如是什么意思
- 人的气派和品貌是什么意思