磷lín
❶色澤鮮明貌。見“磷磷”。
❷象聲詞。見“砰磷”。
磷
读音l·in(ˋ),为in韵目,属en-in-un-ün韵部。良刃切,去,震韵。
❶薄;特指因磨损而变薄。《论语》:“磨而不磷。”
磷
读音l·in(ˊ),为in韵目,属en-in-un-ün韵部。力珍切,平,真韵。
❶[磷磷]水中现石貌。《广韵》:“……水在石间,亦作磷。”。
❷[磷磷]形容玉石的色泽。
❸非金属元素,符号P。
❹磷火;鬼火。
磷林lǐn
薄;薄石。例:板薄~~的。
❍ 他为人薄~,不好交。
《广韵》:“磷,薄石。”何晏注:“磷,薄也。”
磷
〔lin〕 linx。
磷肥〔lin fei〕 linx feix.
磷火 〔lin huo〕 ghunb dongsdeas blaot.


磷*燐粦lín
非金属元素,是生命活动的重要元素,常见的有白磷、红磷
△ ~肥。
磷燐、粦
非金属元素,符号P。常见的有白磷、红磷:~火丨~光丨肥~丨~酸丨黄~丨白~丨红~。
磷lín
非金属元素,符号是P,磷酸盐是重要的肥料之一,磷的化合物可以治疗某些疾病。
磷lin
磷肥 磷光 磷火 磷酸 磷脂 白磷 红磷 卵磷脂
亦作“䗲”,亦稱“景天”。即螢火。《詩·豳風·東山》“熠燿宵行”漢·毛亨傳:“燐,螢火也。”《廣雅·釋蟲》:“景天,螢火,䗲也。”王念孫疏證:“螢,一作熒,䗲,一作燐。”晉·崔豹《古今注·魚蟲》:“螢火……一名景天。”
云母【同义】总目录
云母云英云沙日精云华云精磷
磷
云母的别名。明·李时珍《本草纲目·金石一·云母》:“云华、云珠、云英、云液、云砂、磷石。”
磷lín
〖名词〗
磷火(1)。《祭石曼卿文》:走磷飞萤。——游动着星星磷火,飞舞着点点流萤。
磷燐lín
磷火。欧阳修《祭石曼卿文》:“奈何荒烟野蔓,荆棘纵横,风凄露下,走~飞萤。”
另见359页lìn。
磷lìn
薄,减损。《论语·阳货》:“不曰坚乎?磨而不~。”
另见357页lín。
磷*△燐;粦
C1D7
(一)lin❶一种非金属元素,符号P。白磷、红磷是常见的同素异形体。白磷为淡黄色结晶体,有剧毒,燃烧时产生浓烟,可用于制作烟幕弹或燃烧弹。红磷为暗红色粉末,无毒,可用于制作火柴及各种磷化物。磷酸盐是重要肥料之一。磷的化合物可治疗佝偻病、软骨病等。
❷[磷磷]linlin 1.形容水、石明净的样子:泛泛东流水,~水中石(《文选》)。2.形容玉石色彩鲜明的样子:~烂烂,采色澔汗(《汉书》)。
(二)lin❶薄:不曰坚乎?磨而不~(《论语》)。
❷瑕疵;玷污:明鉴有皎洁,澄玉无~缁(孟郊诗)。
❸畅通:漏管有时而塞,有时而~,则缓急异(徐光启文)。
元素
素(色~;激~;尿~;毒~) 原质
化学元素:碳 磷 硫 硒 碲 硅(矽)砷(砒) 碘 砹 硼 镉 鉫(镓)
气体元素:氮 氧 氟(砩) 氯 氦 氖氩 氪 氙 氡 氰 氢 氕 氘氚 氨
放射性元素:铀 钍 锕 钷 钚 锔 钔 锎 镅 镎 锫 锿 镄 锘铹 钋 钅卢 焊 锝 镭 铀
稀土元素:铈 镧 镨 钕 钐 钷 钆钇 钬 铥 镱 镝 销 铽 铒
主族元素:锂 钠 钾 铷 铯 钫 铜金
铂族元素:钌 铑 钯 锇 铱 铂
金属元素:铪 铼 铊 铟 镓 锗 钠
非金属元素:硒 砷 溴
硫磺:硫 磺
硫黄的别称:黄牙 黄芽
(化学上指具有相同核电荷数的同一类原子的总称:元素)
磷
磷和钙大部分结合在一起,以磷酸钙的形式存在于骨骼和牙齿中(约占机体总磷量的80%)。其余的磷是软组织结构的重要成分,并参与细胞核的组成,RNA和DNA含磷,细胞膜的脂质含磷。糖类的吸收与中间代谢均需磷酸化合物作为桥梁。三磷酸腺苷和磷酸肌酸中的磷尚具有储存及转移能量的作用。磷广泛存于动植物食品中,一般不易缺磷。婴儿喂养若能满足其钙的需要,磷也能满足需要。幼儿的食物更加广泛,磷的来源不成问题。凡是蛋白质含量丰富的食品,磷的含量也丰富,如肉类、蛋类、花生等。维生素D可促进磷的吸收,缺乏维生素D,血磷下降,故佝偻病活动期,血清钙稍低,血磷明显降低,钙磷乘积亦低(30),正常钙磷乘积大于40。
磷
磷是人体必需元素之一,在成人体内含量600~900g,约为人体重量的1%。人体中87.6%以上的磷存在于骨骼和牙齿中。
磷lin
第三周期VA族元素,符号P。1669年德国的H.布朗德由人尿中制出一种蜡状白色固体,即白磷。它具有大蒜味,黑暗中发光,H.布朗德认为这是火素,称为冷火。这一发现引起当时许多科学家的重视,德国医生J.D.克拉夫特购买了这一制取磷的秘密,并在欧洲好几个国家宫廷和富翁住宅里表演在黑暗中磷不断发光的实验,获利不小。英国著明科学家R.波义耳在宫廷里看到表演,后来也知道了从尿中制磷的秘密,并报告给英国皇家学会,直至1694年他去世后才公布了他的制磷方法——用尿和砂子混合蒸馏。A.L.拉瓦西把磷列入元素行列,其拉丁名为phosphorum,英文名phosphorus意为“发光物”。早在我国东汉时期,王充的《论衡》 中对磷就有描述,称为“燐”,即“鬼火”的意思,近代根据我国化学元素的命名原则改为“磷”。磷在地壳中含量较多,其丰度为0.11%,比氮多3.7倍。但它不是以单质而是以化合物形式存在,主要有磷酸钙矿Ca3(PO4)2和磷灰石矿Ca5F(PO4)3,即3Ca3(PO4)2·CaF2。磷也是一种生命元素,组成细胞核的核蛋白是蛋白质和核酸的结合体,核酸的组分核甙酸内就含有各种以磷酸形式存在的磷元素,另外在脊椎动物骨骼中也含有磷酸钙。
磷与碳相似,有几种同素异形体,常见的是白磷、红磷和黑磷,白磷有两种 (但晶体结构不同),红磷和黑磷或为无定形物或为晶体。白磷在空气中很易氧化,因着火点 (燃点) 较低,故在空气中能自燃,在暗处会发生磷光。为了防止白磷的氧化,必须把它保存在水中,磷燃烧时生成五氧化二磷或十氧化四磷。黑磷不易着火,磷在黑暗处发光,这是由于磷所放出的微量蒸气所致,在34℃时着火,60℃时在空气中自行燃烧,并产生白色烟雾,是反应的能量以光的形式放出的缘故。白磷有恶臭味,剧毒! 白磷几乎不溶于水,难溶于乙醇和甘油,较易溶于二硫化碳和苯等。白磷在密闭容器中隔绝空气加热到260℃就逐渐转变为红磷 (是制备红磷的方法)。在转变过程中有热量放出,故红磷较白磷稳定,但反应生成物是相同的。红磷是红棕色粉末,也称赤磷,无毒,不溶于水,略溶于无水乙醇,不溶于其他有机溶剂。白磷在较高气压下加热则变为略有金属性的黑磷或紫磷,它不溶于普通溶剂中。
磷易和氧、卤素等直接化合,也能和某些金属化合生成磷化物,如磷化镁Mg3P2,磷化钙Ca2P2等,这些磷化物水解可得到和氨相似的磷化氢。在电石碳化钙中因夹杂有少量的磷化钙和硫化钙,当将电石与水反应制乙炔时,就常有磷化氢和硫化氢放出,使人误认是乙炔的臭味。磷主要形成+Ⅰ,+Ⅲ和+Ⅴ氧化态的化合物。在含磷的化合物中,磷原子常通过氧原子而和别的原子或基团相联结,白磷常用来制造磷酸、燃烧弹和烟雾弹,红磷用于制造农药 (如有机磷杀虫剂) 和安全火柴。单质磷可由磷酸钙、石英砂和炭粉的混合物在电弧炉中熔烧来制取。
磷lin
磷和钙大部分结合在一起,以磷酸钙的形式存在于骨骼和牙齿中(约占机体总磷量的80%)。其余的磷是软组织结构的重要成分,并参与细胞核的组成,RNA和DNA含磷,细胞膜的脂质含磷。糖类的吸收与中间代谢均需磷酸化合物作为桥梁。三磷酸腺苷和磷酸肌酸中的磷尚具有储存及转移能量的作用。磷广泛存在于动植物食品中,一般不易缺磷。婴儿喂养若能满足其钙的需要,磷也能满足需要。幼儿的食物更加广泛,磷的来源不成问题。凡是蛋白质含量丰富的食品,磷的含量也丰富,如肉类、蛋类、花生等。维生素D可促进磷的吸收,缺乏维生素D,血磷下降,故佝偻病活动期,血清钙稍低,血磷明显降低,钙磷乘积亦低 (<30),正常钙磷乘积大于40。
磷phosphorus,P
系一种非金属元素。原子序数15,原子量30.97。是人体必需元素之一,参与人体骨骼、神经组织、脂类、细胞膜、酶类的组成,以及机体的能量转换、肌肉活动、新陈代谢、电解质平衡及多种生物化学作用等。磷亦是其他生物界重要组成部分,对各种生物的生长、发育、新陈代谢、生命活动均有重要意义。磷在农业生产上有重要意义,可制造多种肥料及农药、在化工生产上亦有重要意义,放射性磷可用于诊断与疾病的治疗。
磷Lin
第15号化学元素,符号P,原子量30.97,天然界没有单质磷存在,多以磷酸盐存在,将磷酸钙、焦炭、硅石在电炉内高温熔化,可以得到白磷: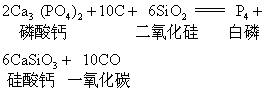
白磷亦称黄磷,分子式P4,淡黄色蜡状固体有大蒜臭味,有毒,熔点44.1℃。沸点280℃,相对密度1.82。不溶于水,易溶于二硫化碳,可溶于苯和乙醇。白磷易燃,在空气中34℃即自行燃烧,应贮存于水中。
白磷隔绝空气加热即转化为红磷,红磷亦称赤磷,为紫红色无定形粉末,有金属光泽熔点590℃,相对密度2.2,红磷无毒无臭,不溶于水,也不溶于二硫化碳,在空气中200℃以上时燃烧(见彩图)。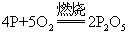
磷的重要化合物有五氧化二磷P2O5,磷酸H3PO4等,生物体内许多重要物质含磷,如磷脂、核酸等。磷是植物生长三要素之一。
磷燐、粦lín
一种非金属元素,符号P,同素异形体有黄磷(白磷)和红磷。黄磷有毒,燃烧时生浓烟,可做烟幕弹和燃烧弹。红磷无毒,可制安全火柴。
磷phosphorus
它与钙是构成骨骼和牙齿的重要材料,也是构成组织细胞中,如核酸、磷脂和某些辅酶的原料,它在三磷酸腺苷和磷酸肌酸中具有储存和转移能量的作用。碳水化合物和脂肪的吸收与中间代谢,均需磷酸化合物存在。磷酸盐从尿中排出的数量和形式可以调节机体的酸碱平衡。
磷
磷和钙一样,也是构成骨胳和牙齿的重要材料。正常成年人骨中磷的总量约为600~900g,约占机体总磷量的80%。磷尚是软组织结构的重要成分,如很多结构蛋白质含磷,RNA和DNA含磷,细胞膜的脂质含磷。磷不仅是构成组织的成分,且有许多非结构性功能,如糖类的吸收与中间代谢均需磷酸化合物作为桥梁。三磷酸腺苷和磷酸肌酸中的磷尚具有储存及转移能量的作用。磷酸盐从尿中排出的量和形式是机体调节酸碱平衡的手段之一。
磷广泛存在于动植物组织中。其存在形式主要是与蛋白质、脂肪结合成为核蛋白、磷蛋白及磷脂等;也有少量其他形式的有机和无机磷酸盐。除植酸形式的磷不能被机体充分吸收和利用外,其他大都能为机体所利用。谷类种子中主要为植酸形式的磷,可利用率低;但当用酵母发酵时,或预先将谷粒浸泡于热水中,则可大大降低植酸磷的含量而增高无机磷酸盐的含量,从而提高其吸收率。磷的吸收,也需要维生素D的协助。维生素D缺乏,常使血清无机磷酸盐下降,故佝偻病患儿常血清钙正常而血清无机磷较低。
我国和其他许多国家都未明确规定磷的供给量,原因是一岁以下的婴儿只要能按正常要求喂养,钙能满足需要,磷必然也能满足需要;一岁以上的幼儿以至成人,由于所吃的食物广泛,磷的来源不成问题,故实际上没有规定磷供给量的必要。一般情况下,若一个人摄入钙和蛋白质足够,则所得到的磷也能满足需要。
磷
磷是体内含量较多而又次于钙的第六位元素,占体重代谢活动,缺磷可导致佝偻病并影响代谢功能。体内磷代谢平衡决定于消化道对磷的吸收及肾脏对磷的排泄,以及骨中成骨作用与溶骨作用之间的动态平衡。此种代谢与钙代谢之间关系密切,它们并相互制约,主要均受活性维生素D、甲状旁腺素及降钙素的调节。
成人体内含磷约600~700g,其中80~90%在骨、齿等硬组织中,与钙结合形成羟磷灰石结晶而存在; 其余的磷主要在软组织细胞中,总量可达100g,以肝、脑、肾以及红细胞中浓度较高,心肌和骨胳肌中较少,在细胞中,磷主要以有机磷酸酯及磷酯等形式存在,在物质代谢中各有不同的功能,血液中磷与血钙之间也有互相制约的关系。
成人体内磷的分布
| 部位 | 磷含量 (g) | 占总量 % | 部位 | (g) 磷含量 | 占总量 % |
| 骨胳 | 600 | 85 | 软组织 血 浆 | 100 2 | 14 0.3 |
| 牙齿 | 3 | 0.4 | 组织间液 | 0.2 | 0.03 |
磷的代谢功能 磷是骨盐的主要成分,并能加强成骨细胞活性,以利成骨。在各种体液中,磷酸盐组成缓冲偶,以维持细胞内外的酸碱平衡。在细胞内物质代谢中,磷酸基团存在于多种有机磷酸酯中。从核酸到蛋白质合成的整个基因表达过程,各步骤皆有各种磷酸酯的生成与作用,如各种核酸、核苷酸等; 磷酸基团是重要的蛋白质化学修饰基团,对蛋白质功能影响很大。在能量代谢过程中,不仅氧化磷酸化以形成高磷酸键为核心问题,物质分解代谢如糖的分解也必须产生多种磷酸酯,各种辅酶常以磷酸酯形式存在,故磷在调节能量代谢中是很重要的。红细胞内糖代谢过程中产生的2,3-二磷酸甘油酸能调节血红蛋白的携氧功能,影响组织供氧。膜上磷脂则能调节多种酶的活性,如 (Na+一K+)ATP酶等,对于维持各种亚细胞结构的功能相当重要。磷的吸收 正常人每天饮食中含磷约1g,大多食物中以有机磷酸酯为主,奶类中大多为无机磷酸盐。有机磷酸酯先经磷酸酶消化而后吸收,一价无机磷酸盐H2PO4-为主要吸收形式,其在肠中的吸收部位较钙的为低,正常吸收率可达60~65%。消化液也含磷,以唾液及胆汁中浓度较高,消化道中内源性磷与食物磷有同样吸收率,粪中排出内源性磷平均为每天100mg。肠道吸收以十二指肠及空肠较强,回肠较差,结肠更差,大部分磷在空肠吸收。磷吸收有赖于Na+的存在,由肠粘膜细胞刷状缘上特异载体结合Na+及H2PO4-后,共同转运入细胞内,Na+通过钠泵转运出细胞侧间隙,需耗能,H2PO4-则通过电位差扩散到细胞外液中而完成吸收过程。食物缺钠盐,显著影响磷的吸收,细胞外液中K+多,则有利于磷的吸收。镁或铝制酸药物在肠道内能与磷酸盐结合而抑制磷酸吸收,有降低血磷的作用。如食物中的钙过多则在pH大于6.0~6.5时可与无机磷结合成沉淀。也会影响磷的吸收。此吸收过程需要耗能,而缺氧,代谢抑制剂如氰化物、亚砷酸盐、2,4二硝基酚等都会强烈抑制磷的吸收。
在肠中,1,25二羟维生素D3能有效地促进磷的吸收,近来发现此种作用并不依赖于钙的吸收,而是直接增强了粘膜细胞对磷的转运。甲状旁腺素也有促进肠道中磷吸收的作用,故甲状旁腺功能亢进者磷吸收加强。
磷的排泄 食物中磷在消化道吸收后,可有10%随消化液分泌再经粪便排出; 其余90%吸收的磷皆经肾脏排泄。肾脏是排泄磷的主要脏器。血浆通过肾小球,有90%无机磷滤过基底膜,每天总量可达5g; 其中85~90%为肾小管重吸收,近曲小管重吸收占60~70%,前半部分作用较强,远曲小管及集合管的重吸收占10~25%,各部分重吸收机理不完全相同。未被重吸收而随尿排出者占5~20%,平均每天排出无机磷650mg。近曲小管重吸收无机磷时,由肾小管细胞膜刷状缘上的特异载体结合Na+与H2PO4-,转运到细胞内,再扩散入血液,故Na+的重吸收常伴随着磷的重吸收;原尿中HCO3-增多时,pH升高,尿呈碱性,可使无机磷呈HPO42-的两价形式而不易被重吸收,可增强尿磷排泄; 远曲小管中磷的重吸收与Na+的重吸收无关。
肾小管细胞内无机磷含量多会影响磷的重吸收。体内缺磷则重吸收加强而尿中排磷少; 进食磷多,则增加尿磷的排泄。甲状旁腺素是促进尿磷排泄的主要激素,它能抑制近曲小管对原尿中的无机磷,Na+、HCO3-的重吸收,而HCO3-在原尿中增加又间接抑制无机磷的吸收; 同时甲状旁腺素尚能抑制远曲小管对磷的重吸收而不影响对Na+的重吸收。因此它通过多种方式促进了尿磷的排泄。由于甲状旁腺素的分泌受低血钙调节,过多的甲状旁腺素可促进骨盐溶解而升高血钙和血磷,同时又促进了尿磷的排泄,对于维持血钙恒定而防止血磷升高具有重要意义。活性维生素D则能促进肾小管中磷的重吸收而减少尿磷的排泄,对维持血磷具有重要意义。
降钙素也能使人体尿磷增加,但机理不明。肾上腺糖皮质激素及雌激素能降低肾小管对磷的重吸收而促进排泄; 甲状旁腺素及生长素则能增强肾小管对磷的重吸收而减少磷从尿中排泄。
肾小球功能障碍会妨碍无机磷的滤过而影响尿中磷的排泄; 滴注盐水可抑制近曲小管对Na+及水的重吸收,磷的重吸收也受影响,而尿中排泄增多。当肾小管功能障碍而影响磷的重吸收时,尿磷排泄增多,严重时可致血磷降低,导致肾性佝偻病。
血磷 血细胞中的磷主要以磷酸酯及磷脂存在。血浆中磷也有2/3以上为有机磷,大部分为磷脂,10%以下为其他磷酸酯,共约80mg/L;其余1/3为无机磷,通常所称血磷系指血清中无机磷而言,正常成人血清无机磷约0.7~1.4mmol/L(2.2~4.4mg/dl),变动范围较钙大。婴儿血磷浓度较高,随年龄增长而下降; 又有昼夜周期,每天早晨较低而傍晚升高;进食糖类时血中浓度下降,可能是葡萄糖等进入细胞增强形成较多有机磷酸酯所致。
正常人血中无机磷存在形式

小部分血磷与血浆蛋白质结合; 大部分呈各种离子状态或与金属离子结合而存在,这部分称为可扩散性磷。
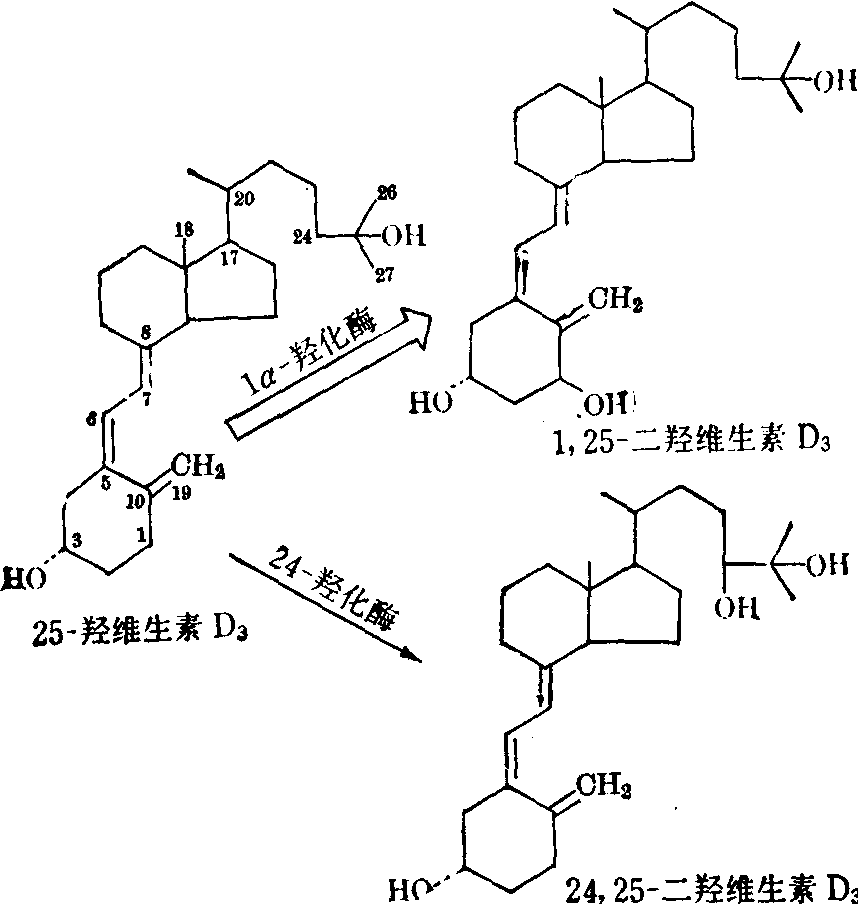
1,25二羟维生素D3是调节血磷的主要因素。在肾脏中,可使肝脏中生成的25羟维生素D3经1α羟化酶作用,羟化形成1,25二羟维生素D3。血磷下降时,肾中1α羟化酶活性增强,使1,25二羟维生素D3生成增多; 血磷升高时,则肾中24羟化酶活性升高,产生24,25二羟维生素D3。对钙、磷代谢无明显作用。
1,25二羟维生素D3既能促进骨吸收而增加骨盐溶解,又能促进消化道对磷的吸收,也能增强肾小管对磷的重吸收而减少尿磷的排泄,因此有效地升高了血磷,以维持血磷浓度的恒定。由于在维生素D活性代谢产物作用下,血钙也会升高,可抑制甲状旁腺素的分泌,也间接减少了尿中磷的排泄,对维持血磷浓度有重要意义。
许多激素主要通过肾脏排泄磷功能的改变而调节血磷的浓度。前述甲状旁腺素主要通过抑制肾小管对磷的重吸收而促进磷排泄以维持血磷恒定,此种作用较强。肾上腺糖皮质激素、雌激素也有类似作用,但较弱; 甲状旁腺激素除了加强骨的吸收外,还能促进磷的重吸收而升高血磷; 它们都可能在影响血钙的基础上改变甲状旁腺素的分泌,间接导致血磷改变。生长素也能促进肾小管重吸收磷而使血磷升高,故新生儿及儿童的空腹血磷浓度高于成年人。
磷phosphorus,P
人体内无机元素之一。原子量30. 9738,原子价3,5。其生理功能主要以磷酸根的形式参与许多对生命活动非常重要的物质代谢过程。如构成磷脂,进而与蛋白质结合,构成细胞膜的组成成分,参与能量代谢,尤其是氧化磷酸化过程,形成ATP等;参与DNA、RNA及许多辅酶的构成。它还在维持体液酸碱平衡中起缓冲作用,及调节维生素D的代谢等。成人体内磷的总含量为400~800g,约87.6%以上的磷存在于骨骼和牙齿中,其余的磷大部分构成软组织成分,小部分存于体液中。磷的吸收部位在小肠上段,经肾及肠排泄。正常成人血磷为3~4.5mg%(1.0~1.5mmol/L),儿童为4~7mg%(1.3~2.3mmol/L)。增高见于甲状旁腺功能减退、肾衰、多发性骨髓瘤、维生素D 摄入过多、骨折愈合期;降低见于甲状旁腺功能亢进、佝偻病、骨质软化症、 脂肪泻、肾小管变性病变、糖尿病等。
磷lín
{化} (非金属元素) phosphorus (P): 白 ~ white phosphorus; 红[赤] ~ red phosphorus; 黄 ~ yellow phosphorus; 紫 ~ violet phosphorus
◆磷蛋白 phosphoprotein; 磷肥 {农} phosphate fertilizer; 磷光 {原物} phosphorescence; 磷光体 phosphorus; phosphor; 磷化合物 phosphorus compound; 磷火 will-o'-the wisp; phosphorescent light; 磷矿粉 {农} ground phosphate rock; 磷燃烧弹 {军} phosphorous bomb; 磷酸 {无化} orthophosphoric acid; phosphoric acid; 磷酸盐 {化} phosphas phosphate; phosphate; 磷虾 krill; euphausiid; 磷盐 microcosmic salt; sodium ammonium hydrogen phosphate; 磷脂 lipoid; lipin; phospholipid; phosphatide; phospholipins; 磷脂酸 phosphatidate; phosphatidic acid; 磷中毒 phosphorism
磷
phosphorus (P)
磷.jpg) 金文;《説文》所無lín
金文;《説文》所無lín
[石(意符)+粦(聲符)→磷(一種非金屬元素,常見的有“白磷”和“紅磷”:磷火,俗稱鬼火。)]
[東漢] 王充《論衡·論死》:“磷,死人之血也,其形不類生人之形也。”
磷*燐;粦lín
(17画)![]()

【提示】米,中间是竖,不是竖钩。 ,3画,第二笔是竖折,旧字形断成一竖、一横。
,3画,第二笔是竖折,旧字形断成一竖、一横。
*磷〔粦 燐〕lín
17画 石部 非金属元素,符号P。常见的有白磷(黄磷)和红磷(赤磷)。白磷为淡黄色结晶,有剧毒,易在空气中氧化,燃烧时产生浓烟,可制烟幕弹和燃烧弹。红磷为暗红色粉末,无毒,可制安全火柴。
磷燐粦lín
古代作粦。小篆上从炎,隶楷讹作“米”;下从舛(chuǎn),是人的两足(止字旁的变形)。本读去声。《说文》说是“鬼火”。如:磷火。中古时因隶楷“炎”在上部讹变“米”,字义不显;加火旁作燐。古代又有粼(lín)字,形容水、石等明净。中古因右旁两折笔(浍(kuài)本字)生僻,造磷,从石旁。现代科学认为磷是一种非金属元素。常见的有白磷(也叫黄磷)和红磷。白磷有毒,可作军事上用的烟幕弹和燃烧弹。红磷无毒,可制安全火柴。磷是植物营养的重要成分之一。现以磷为规范字。其他两字作异体字。见《异体字表》。粼少用,未收。
磷粦★异◎异;燐★异◎常★常◎常

lín粦,表意,金文、小篆从炎从舛(chuǎn),炎指火星,舛象人的两足,表示行走,隶定字形把炎讹为米。本义为随风飘动的磷火(是“磷”的本字)。磷,形声,从石,粦声,本义为山石间的水清澈(与“粼”同),假借为磷火、一种非金属元素等。燐,形声,从火,粦声,磷火。《异体字表》以“粦”“燐”为异体字。
【辨析】
❶“磷、粦、燐”不是等义异体字。
❷以“粦”作音符构成的形声字一般读lin,但声调不同。lín:磷、鳞、嶙、遴、辚、瞵、粼、麟∣lìn:膦。
【构词】
磷肥(磷肥)∣磷光(磷光∕燐光)∣磷火(磷火∕燐火)
- 番是什么意思
- 番是什么意思
- 番是什么意思
- 番上是什么意思
- 番丙药是什么意思
- 番业户是什么意思
- 番乙是什么意思
- 番九是什么意思
- 番云纱是什么意思
- 番五是什么意思
- 番人是什么意思
- 番人正是什么意思
- 番人酵是什么意思
- 番仔是什么意思
- 番仔哥是什么意思
- 番仔姜是什么意思
- 番仔婆是什么意思
- 番仔字是什么意思
- 番仔松柏是什么意思
- 番仔柿是什么意思
- 番仔桃是什么意思
- 番仔楼是什么意思
- 番仔正是什么意思
- 番仔油是什么意思
- 番仔火是什么意思
- 番仔灰是什么意思
- 番仔狗是什么意思
- 番仔番薯是什么意思
- 番仔码是什么意思
- 番仔码子是什么意思
- 番仔肥是什么意思
- 番仔芋仔是什么意思
- 番仔芦荟是什么意思
- 番仔菜是什么意思
- 番仔薯是什么意思
- 番仔蜡是什么意思
- 番仔衫是什么意思
- 番仔饼是什么意思
- 番仔麦是什么意思
- 番代是什么意思
- 番仲是什么意思
- 番仲戈是什么意思
- 番休是什么意思
- 番佛是什么意思
- 番僧寺是什么意思
- 番僧源流考是什么意思
- 番兜是什么意思
- 番兜城是什么意思
- 番兵是什么意思
- 番典是什么意思
- 番割是什么意思
- 番包是什么意思
- 番包萝是什么意思
- 番匏是什么意思
- 番匠是什么意思
- 番单是什么意思
- 番叟是什么意思
- 番号是什么意思
- 番司是什么意思
- 番名是什么意思