氮同化nitrogen assimilation
植物体内无机氮(NO-3、NH+4、N2)转化为有机态氮(氨基酸、蛋白质)的过程。大多数植物从土壤中吸收NO-3和NH+4,而某些与各种微生物共生的植物,除了吸收这些无机氮外,还能利用大气中的N2,它们在植物体内都同化为有机氮。此外,植物还能直接吸收一些有机态氮如氨基酸、酰胺、尿素,并同化为多种有机氮化合物。
硝酸盐的还原 进入植物体内的硝酸盐在其被同化为氨基酸之前,必须还原成NH3,这个过程称为硝酸盐还原。参与该过程的两种酶是硝酸还原酶和亚硝酸还原酶,前者将NO3-还原成NO2-,后者将NO2-还原为NH3。在光照条件下绿色植物叶细胞中NO3-同化的基本机理见图1。
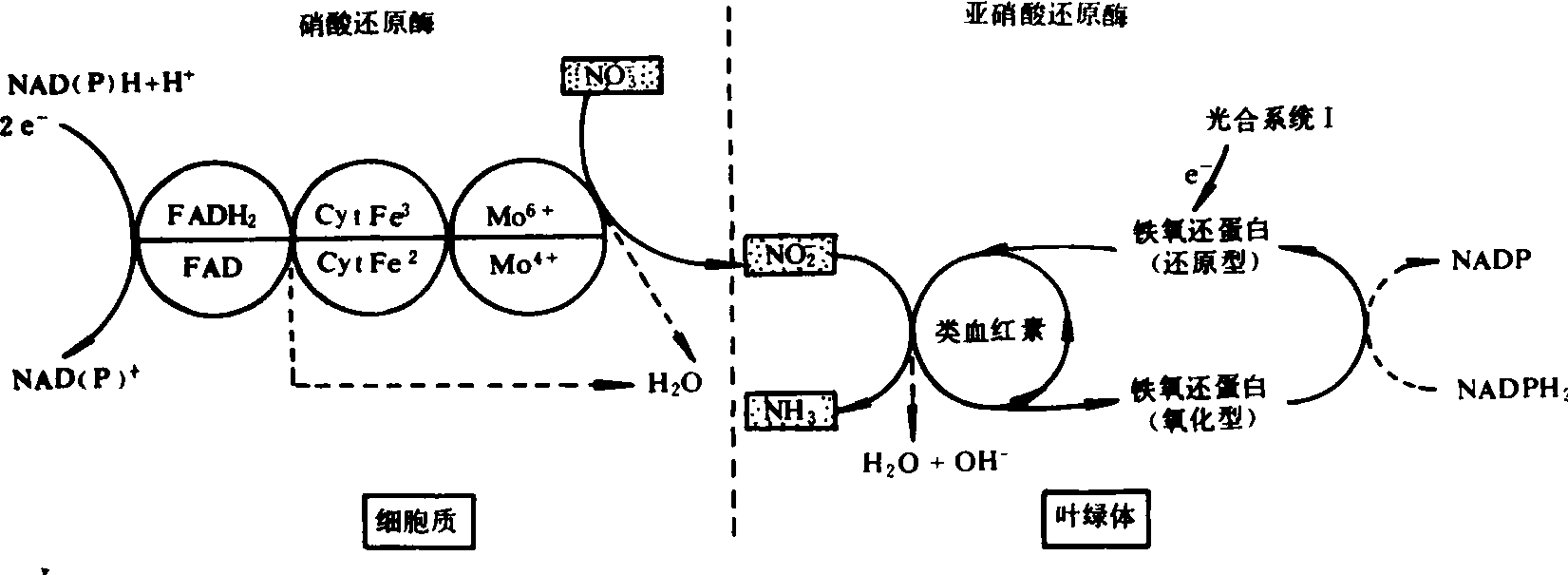
图1 叶细胞中硝酸盐同化的顺序图式
硝酸还原酶是一种底物诱导酶,在高等植物体内其分子量约为200 000,在低等植物中达500 000。它含有几种辅基,包括黄素腺嘌呤二核苷酸(FAD)、细胞色素b(cytb)和钼。该酶位于高等植物细胞的细胞质内,需要还原态烟酰胺腺嘌呤二核苷酸(NADH)或还原态烟酰胺腺嘌呤二核苷酸磷酸(NADPH)作为电子供体。先是由NADH或NADPH将电子传递给FAD,使FAD变为FADH2,电子再通过FADH2转移到细胞色素b,再由细胞色素b转移到钼,最后电子直接从钼转移到NO3-,使之还原为NO-2。在植物体内硝酸还原酶的半衰期仅几小时,其酶蛋白合成一分解速率很快,在含量很低时,不能接受硝酸盐。但在介质中供给硝酸盐和加入细胞分裂素时,在几小时内植物体内能诱导产生这种酶。所以其活性随硝酸盐含量而增加,与氮素供应关系密切。硝酸还原酶的活性能被铵及某些氨基酸或酰胺所抑制。
绿色组织中亚硝酸还原酶位于叶绿体内;根内的亚硝酸还原酶存在于前质体中。在绿色组织中,NO-2还原的电子供体是还原态铁氧还蛋白(Fdred),铁氧还蛋白(Fd)在光下通过光系统I接受电子而呈还原态。
亚硝酸还原酶催化的反应如下:
![]()
铁氧还蛋白一亚硝酸还原酶是由600个氨基酸残基组成的单一多肽链,其分子量较小,约为62 000。它含有两个辅基,一为四核的4Fe-4S铁硫中心,另一个为含血红蛋白的类血红素(sirohem)。通过亚硝酸还原酶,从还原态铁氧还蛋白到亚硝酸的电子传递途径,可概括如下:
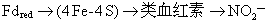
还原态铁氧还蛋白使类血红素还原,然后类血红素结合一个NO2-成为类血红素-NO2-复合物,复合物的形成促进铁硫中心接受Fdred的电子被还原,然后铁硫中心再把电子传递给类血红素-NO2-复合物,使NO-2逐步还原,最后形成的NH3释放出来(图2)。
根亦能很快同化NO2-,但根组织中不存在铁氧还蛋白,根的前质体内存在戊糖磷酸途径的酶系统,可产生NADPH,能用于NO2-的还原。在正常条件下,完整植株中很少有NO2-积累,估计是因为植株体内亚硝酸还原酶含量比硝酸还原酶高得多,亚硝酸还原过程速率比硝酸还原过程快的缘故。
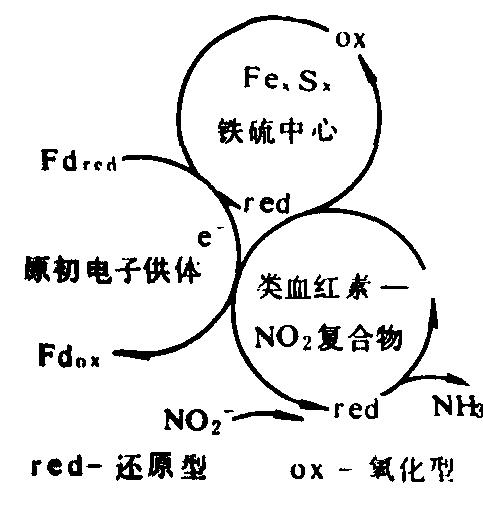
图2 NO-2还原过程
大多数植物不论在根部还是在地上部都能进行硝酸盐还原。在各部位进行还原所占的比例决定于各种因子,包括硝酸盐供应水平、植物种类、植株年龄和植株矿质营养条件等。通常当外界硝酸盐供给水平低时,在根部还原硝酸盐的比例较高;在硝酸盐供应水平较高时,地上部则是硝酸还原的主要位置。
硝酸盐还原的位置还因植物种类而异。木本植物根部进行硝酸盐还原的能力通常很高。在一年生植物中,根部还原NO3-的能力按以下次序递减:油菜>大麦>向日葵>玉米>苍耳。苍耳几乎全部在叶片中同化硝酸盐,这类植物根部不存在硝酸还原酶的活性。在豆科植物中,根部还原硝酸盐的比例(与叶部相比)按以下次序减少:羽扇豆>鹰嘴豆>豌豆>三叶草>大豆。
硝酸还原作用也与植株年龄有关。比较幼嫩植株的正在扩展的幼叶、幼根和根尖,其硝酸还原酶的活性最大;而较老植株其酶的活性则明显衰退。
硝酸还原作用受矿质养分尤其是Mo、Mn、Fe的影响较明显。当植物体内缺乏这些元素时,硝酸盐积累而不易还原。若当伴随的阳离子是K+,则K+和NO3-一起迅速运输到地上部,因此在根部硝酸还原相应地较低;反之,当伴随的阳离子是Ca2+或Na+时,根部的硝酸还原作用就相当高。
其他环境因素如光照强度、水分胁迫、温度、CO2浓度等也能影响硝酸盐还原为铵。硝酸盐在植物体内过多时,储存于液泡中,对植物本身无毒害。但饲料、蔬菜等作物中含过量的硝酸盐,在供家畜和人食用时则是有害的。
氨的同化 根部吸收铵离子,或由硝酸盐还原和分子氮固定产生的氨,都可以与呼吸作用所产生的各种酮酸如a-酮戊二酸、草酰乙酸、延胡索酸等先形成氨基酸,即谷氨酸和天门冬氨酸。
氨的同化可在根、根瘤和叶部进行,在多数情况下参与同化的关键酶都是谷氨酰胺合成酶和谷氨酸合酶(GOGAT途径)。这两种酶在根部、叶绿体和固氮微生物中均有发现。谷氨酰胺合成酶直接催化谷氨酸与氨发生反应,生成谷氨酰胺,其反应如下:
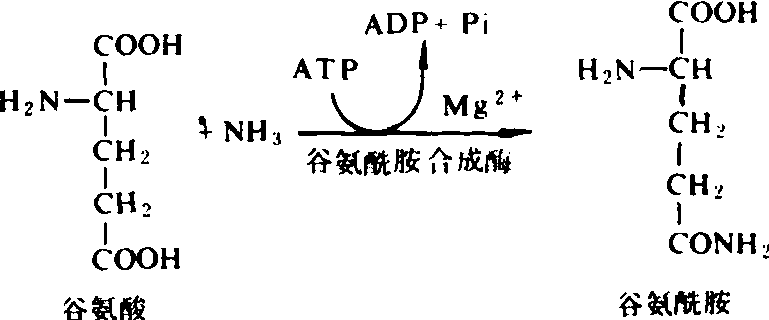
谷氨酰胺合成酶对氨的亲和力很高(Km值低),所以即使在氨浓度很低时,也能与氨结合。叶绿体中谷氨酰胺合成酶的存在,保证了由亚硝酸还原酶形成的NH3浓度维持在很低的水平,不至使光合磷酸化发生解偶联作用。
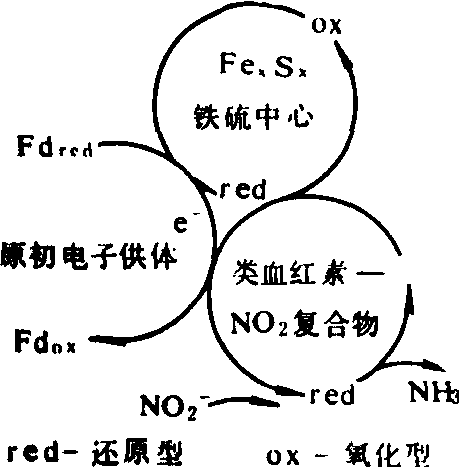
图2 NO2-还原过程
谷氨酰胺合成后,与α-酮戊二酸反应,在谷氨酸合酶的作用下,生成两个分子谷氨酸。其反应如下:
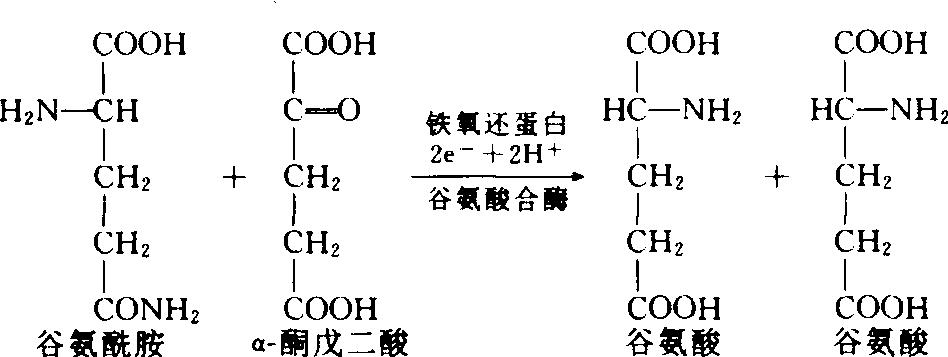
净反应:NH3+α-酮戊二酸+2e-+2H++ATP→谷氨酸+ADP+Pi
以上反应属吸能过程,需要pH值高,也需要Mg2+和ATP的浓度高,并由还原态铁氧还蛋白(来自光系统Ⅰ)或NAD(P)H(来自呼吸作用)提供所需要的还原力。反应产生的两个分子谷氨酸,其一可维持氨同化循环的需要,另一则可用于蛋白质的生物合成。当氨的供应充足时,则两个分子的谷氨酸均能作为氨的受体,而有一个分子谷氨酰胺留在循环中,以解除游离氨的毒害(图3)。
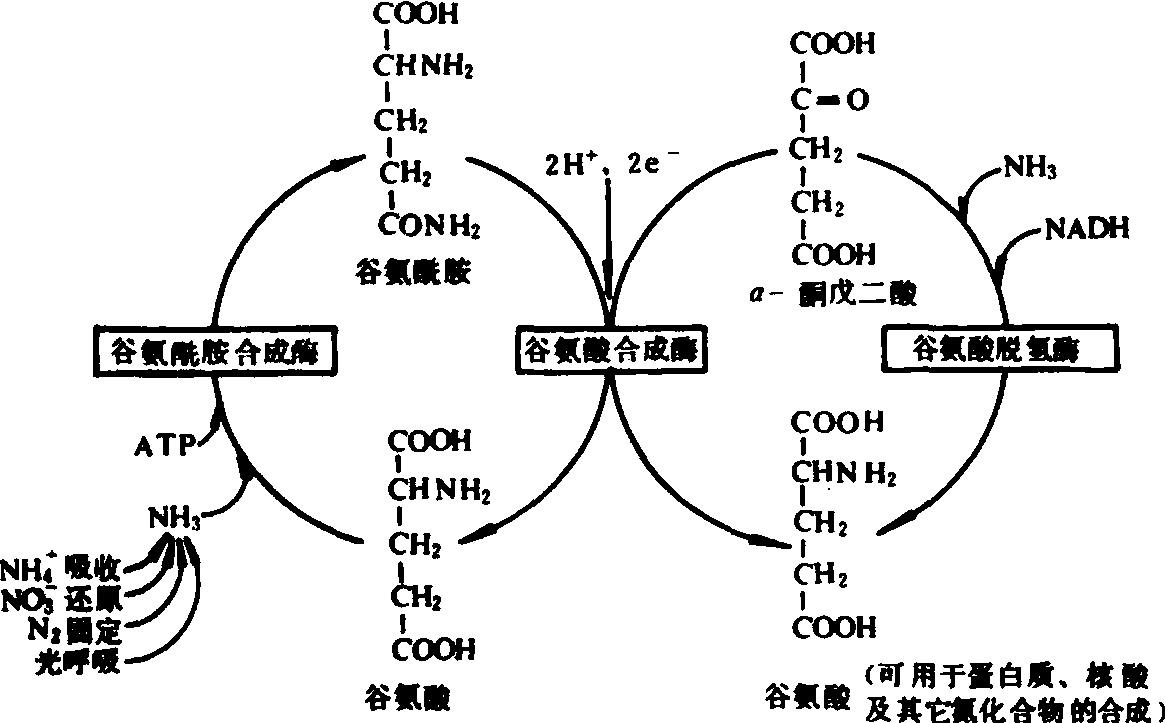
图3 氨的同化途径的模式
在氨的同化中另一途径为谷氨酸脱氢酶(GDH)途径,即在GDH作用下,NH3与α-酮戊二酸结合形成谷氨酸。反应式为:
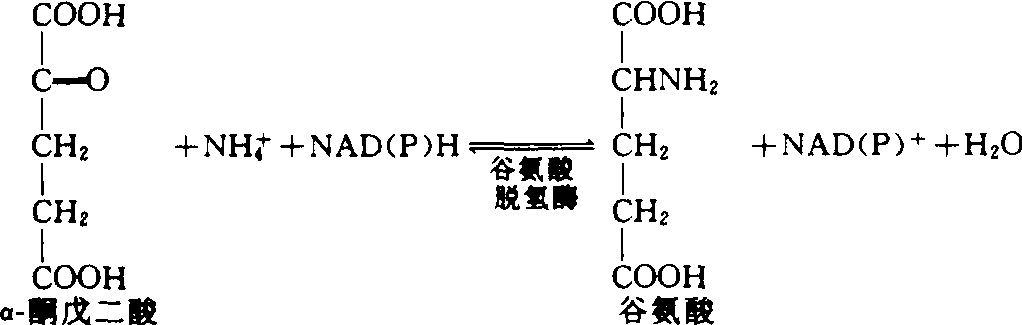
谷氨酸脱氢酶主要位于根和叶细胞的线粒体中,对氨的亲和力低(Km值高),需要较高浓度NH+4才能完成上述反应。在一般情况下,如细胞内氨浓度过高则使光合磷酸化解偶联,所以这一途径不能是氮素同化的主要途径。但是当介质NH+4浓度高,植物体内NH+4积累时,谷氨酸脱氢酶途径对于解氨毒可能有重要作用。
氨基酸和蛋白质的合成氨基酸的合成 谷氨酸和谷氨酰胺能进一步用于合成其它酰胺、氨基酸和蛋白质。合成蛋白质需要20种不同的氨基酸,在蛋白质中各种氨基酸的排列顺序受基因所控制。
谷氨酸中的氨基通过氨基转移作用,传递给其它酮酸,形成其它类型氨基酸。在此反应中起催化作用的酶是氨基转移酶,又称转氨酶。例如:
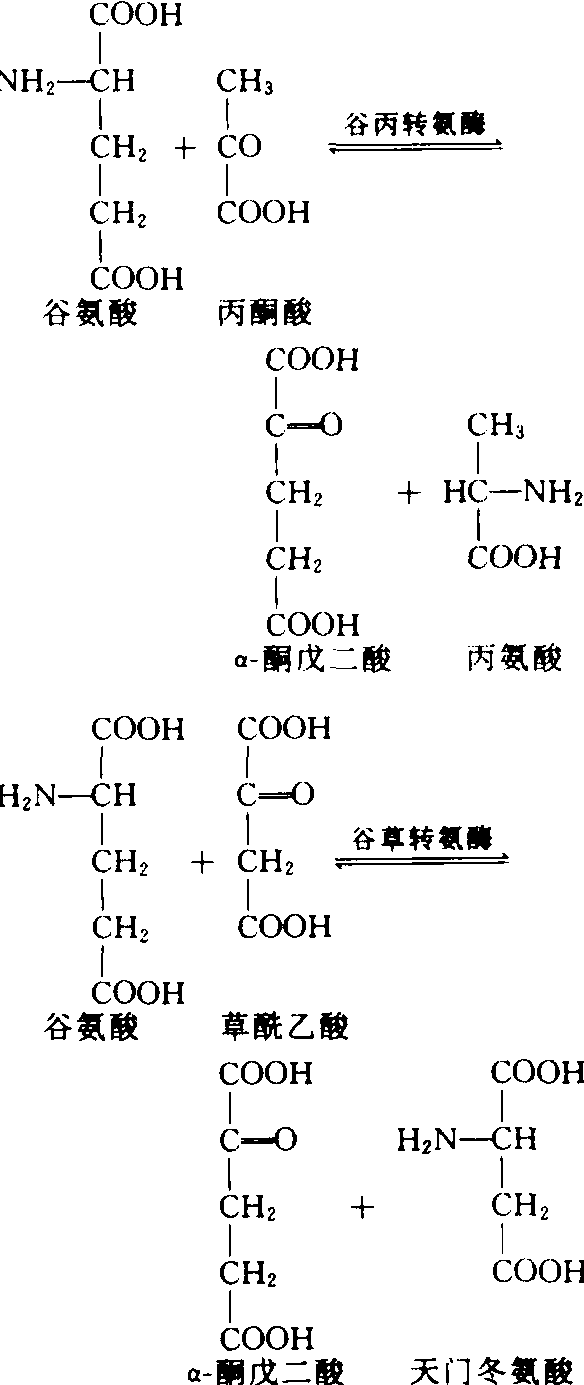
转氨基作用在真核细胞中的细胞质和线粒体中皆有发现。各种转氨酶的辅基都是磷酸吡哆醛,它是维生素B6的衍生物。谷氨酸、天门冬氨酸、丙氨酸和相应的酮酸进行转氨基反应可生成很多种氨基酸,如鸟氨酸、精氨酸,脯氨酸、赖氨酸、苏氨酸、缬氨酸、亮氨酸等。
当NH3过多时,谷氨酸和天门冬氨酸可作为NH3的受体,它们分别在酰胺合成酶的催化下,合成谷氨酰胺和天门冬酰胺。例如:
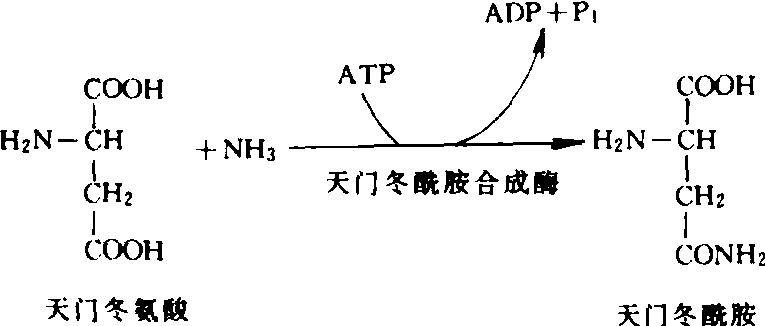
当作物大量施用无机氮特别是铵态氮肥时,植株内经常会有谷氨酰胺和天门冬酰胺的积累,它们能参与氮素代谢,对储存氮素、消除氨的毒害均起重要作用。
蛋白质的合成 是由各个氨基酸之间以肽键连接起来形成多肽链。其缩合反应如下:
![]()
蛋白质是由100个以上单个氨基酸组成的多肽。它们的排列顺序是决定于由脱氧核糖核酸(DNA)分子中携带的遗传信息。遗传信息先转录到信使核糖核酸(mRNA)上,然后再由mRNA转译为多肽链中氨基酸的顺序。
核糖体对蛋白质生物合成的几个特殊阶段是必需的:❶氨基酸活化和氨基酸-tRNA合成;
❷肽链起始和延长;
❸链的终止,肽链和核糖体从多聚核糖体的复合体上释放。在这些过程中矿质养分起重要作用。维持有高度秩序的核糖体结构需要二价阳离子,特别是Mg2+,镁对氨基酸的活化也是必需的;锌是RNA聚合酶的金属成分;而铁在某些情况下对核糖体的结构完整是必需的。
在细胞和组织中,蛋白质的生物合成和降解是同时发生的。这两个过程之间的平衡决定于各种因子,包括不同发育时期(如叶龄)、源—库关系和植物的营养状况。植物激素在调节这一平衡中直接或间接地起支配作用,那些强烈影响植物激素平衡的矿质营养如氮也很重要。到植株生育后期,茎叶中的蛋白质在酶作用下分解,其降解产物主要是氨基酸,转移到正在发育中的花序和果实内,因此,茎叶的净蛋白质含量迅速下降。
- 唐文光是什么意思
- 唐文凤是什么意思
- 唐文君是什么意思
- 唐文宗是什么意思
- 唐文宗吟杜诗是什么意思
- 唐文宗大和七年是什么意思
- 唐文宗大和三年是什么意思
- 唐文宗大和九年是什么意思
- 唐文宗大和二年是什么意思
- 唐文宗大和五年是什么意思
- 唐文宗大和元年是什么意思
- 唐文宗大和八年是什么意思
- 唐文宗大和六年是什么意思
- 唐文宗大和四年是什么意思
- 唐文宗开成二年是什么意思
- 唐文宗开成五年是什么意思
- 唐文宗开成四年是什么意思
- 唐文宗李昂的人物故事|评价|小传,唐文宗李昂的事迹|史鉴是什么意思
- 唐文宗章陵是什么意思
- 唐文宗谐谑是什么意思
- 唐文宗赐鸡是什么意思
- 唐文宗题诗是什么意思
- 唐文巨擘是什么意思
- 唐文恺是什么意思
- 唐文愷是什么意思
- 唐文扆是什么意思
- 唐文扆谋去大臣案是什么意思
- 唐文拾遗是什么意思
- 唐文明判集是什么意思
- 唐文标事件是什么意思
- 唐文治是什么意思
- 唐文渊是什么意思
- 唐文爽是什么意思
- 唐文献是什么意思
- 唐文粹是什么意思
- 唐文粹序是什么意思
- 唐文粹补遗是什么意思
- 唐文续拾是什么意思
- 唐文续拾遗是什么意思
- 唐文选是什么意思
- 唐文选注是什么意思
- 唐文鉴是什么意思
- 唐文高是什么意思
- 唐文魁是什么意思
- 唐斯之战是什么意思
- 唐斯诉比德韦尔案是什么意思
- 唐斯,约翰是什么意思
- 唐新是什么意思
- 唐新书是什么意思
- 唐新语是什么意思
- 唐方妻丁锦孥的人物故事|评价|小传,唐方妻丁锦孥的事迹|史鉴是什么意思
- 唐方镇年表是什么意思
- 唐旄是什么意思
- (唐)无名氏《怨回纥·曾闻瀚海使难通》是什么意思
- (唐)无名氏《竹枝·盘塘江口是奴家》是什么意思
- (唐)无名氏《菩萨蛮·牡丹含露真珠颗》是什么意思
- 唐旧志是什么意思
- 唐时为进士语是什么意思
- 唐时升是什么意思
- 唐时南昭是什么意思