气体定律
气体定律
气体的三个物理量: 体积、压强和温度,叫做气体的状态参量。气体定律就是气体状态参量之间的变化规律。这些定律,对于气体本身的体积和分子间作用力,都略去不计,故对理想气体才能够成立,但也近似反映实际气体的性质。在潜水和潜水医学实践中,无论是潜水供气和配气,还是科学研究和疾病治疗等等,都要用到气体定律进行各种必要的计算。
气体所占容器的容积,就是气体的体积(V)。气体的压强(P)是气体分子不断碰撞器壁在单位面积上所产生的作用力。温度是定量地反映物体冷热程度的物理量。温度的数值表示方法叫做温标。摄氏温标是一种常用的温标 (代号为℃,符号为t)。在气体定律计算中,还用到绝对温标,即以-273℃作为绝对零度,而绝对温标每度的大小,与摄氏温标相同。绝对温标的代号为K,符号为T。它与摄氏温标的关系是T=t+273
Boyle-Mariotte定律:一定质量的气体,在温度保持不变时,它的压强与体积成反比。其关系式为:
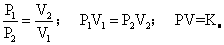
式中K表示常量
Boyle-Mariotte定律在潜水和潜水医学实际中,对了解和计算在不同水深(或压强)处气体的压缩或膨胀,和在供气时气体的压强和体积之间的关系,是很重要的.例如: 在水面一定体积的气体,到水下10m处 (压强由1ATA增加到2ATA),气体的体积压缩到原体积的1/2。在水下20m处一定体积的气体,到水面时(压力由3ATA减少到1ATA),气体体积膨胀到原体积的3倍。
Charles 定律 一定质量的气体,在体积保持不变时,温度每升高1℃,其压强就增加0℃时压强的1/273。关系式为:
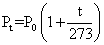
如果温度用绝对温度表示,可得:
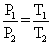
即: 一定质量的气体,在体积不变时,压强和绝对温度成正比。Charles定律在潜水和潜水医学实践中,对了解和计算一定质量和体积的气体在不同温度下的压强变化,有实用意义。例如,一定质量和体积的气体在0℃时的压强为150ATA,当温度升高到54.6℃时,其压强就达180ATA。
Gay-Lussac定律 一定质量的气体,在压强保持不变时,温度每升高1℃,其体积就增加在0℃时体积的
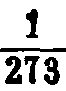 。关系式为:
。关系式为: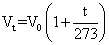
如果温度用绝对温度表示,可得:
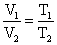
即: 一定质量的气体,在压强不变时,它的体积与绝对温度成正比。
气体状态方程式 当一定质量的气体与外界发生能量交换时,它的三个状态参量往往同时发生变化。可在上述三个定律的基础上,研究气体状态参量的变化规律,得出:
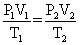
即: 一定质量的气体从状态P1、V1、T1变化到状态P2、V2、T2时,各状态的PV/T的值保持不变。这是气体状态方程式的一种形式。
在标准状况下,1 mol任何气体的体积都是22.4L,即:P0=1ATA,T0=273°K, V0=22.4L,因此,
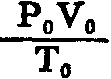 是一个确定的常数,用R表示。对于任何气体,R的值都相同(0.082Atm.L/mol.°K)。所以把R叫做普适气体常数(或通用气体常数)。
是一个确定的常数,用R表示。对于任何气体,R的值都相同(0.082Atm.L/mol.°K)。所以把R叫做普适气体常数(或通用气体常数)。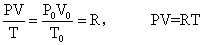
这就是质量为1 mol的理想气体的状态方程式。
对于质量为M克,克分子量为u的理想气体,则为:
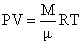
气体的标准化和标准化方程式在医学实践中,为了便于精确地计算和比较,所有在非标准状况下测量或推算出的气体体积,都须应用气体状态方程式换算成标准状况下的体积。这一换算过程称为标准化。
已知在非标准状况下气体体积为V,温度为t,压力为P(习惯上用mmHg表示)。设在标准状况下气体体积为V0。则
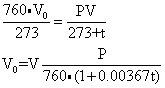
式中P可用气压计在当时当地实测。
在医学实际中得到的气样,常常是饱和了水汽的。因此,在换算时须在压力中减去水汽的分压(W)。方程式即为:
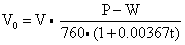
在不同温度下,饱和水汽的分压不同,可从查表取得。为了使用方便,人们把不同压力,不同温度和相应饱和水汽分压下1000ml气体,根据上述计算式换算成标准状况下所占的体积,列表供查找。
在实际使用中,除上述标准状况(STPD)外,还有所谓环境温度和压力、干燥气体(ATPD),环境温度和压力、饱和水汽(ATPS)以及体温和环境压力、饱和水汽(BTPS)等,都可按上述换算式进行相应的换算。
☚ 气体压强及计量单位 气体分压和Dalton定律 ☛
- 国朝闺秀诗柳絮集是什么意思
- 国朝闺阁诗钞是什么意思
- 国朝闺阁诗钞续编是什么意思
- 国朝隶品是什么意思
- 国朝风雅是什么意思
- 国朝馆选录是什么意思
- 国朝骈体正宗是什么意思
- 国朝(明)诗评是什么意思
- 国朝(清)诗人徵略初编是什么意思
- 国朝(清)诗话是什么意思
- 国木是什么意思
- 国本是什么意思
- 国术是什么意思
- 国术与体育是什么意思
- 国术倒流的空手道之秘密是什么意思
- 国术初阶是什么意思
- 国术半月刊是什么意思
- 国术史是什么意思
- 国术名人录是什么意思
- 国术周刊是什么意思
- 国术声是什么意思
- 国术大全是什么意思
- 国术教本是什么意思
- 国术月刊是什么意思
- 国术概论是什么意思
- 国术源流考是什么意思
- 国术理论是什么意思
- 国术省考是什么意思
- 国术示范讲习所是什么意思
- 国术统一月刊是什么意思
- 国术论丛是什么意思
- 国权是什么意思
- 国权比人权重要得多是什么意思
- 国材是什么意思
- 国林之是什么意思
- 国林耀是什么意思
- 国林跃是什么意思
- 国柄是什么意思
- 国柱是什么意思
- 国标是什么意思
- 国标码是什么意思
- 国树是什么意思
- 国格是什么意思
- 国格人格是什么意思
- 国桢是什么意思
- 国梁是什么意思
- 国棉一厂社区是什么意思
- 国棉二厂社区是什么意思
- 国棉五厂唐墓俑是什么意思
- 国棉厂是什么意思
- 国棉四厂唐墓俑是什么意思
- 国棋是什么意思
- 国楹是什么意思
- 国榷是什么意思
- 国槐是什么意思
- 国歌是什么意思
- 国正是什么意思
- 国正人心顺,官清民自安。是什么意思
- 国正天心顺,官清民自安是什么意思
- 国步是什么意思