不可逆电池
不可逆电池bukeni dianchi
参见“可逆电池”。可逆电极 (keni dianji) 构成可逆电池的电极,其电极反应必须是可逆的,称为可逆电极。可逆电极有以下几种类型:
❶ 第一类电极 包括金属电极、氢电极、氧电极、卤素电极等。金属电极是将金属浸在含有该金属离子的溶液中构成,以符号M|M2+表示,电极反应为:
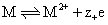
氢电极、氧电极和氯电极分别是由将被H2,O2,Cl2的气流冲击的铂片浸入含有H+,OH-和Cl-的溶液中构成,用符号(pt)H2|H+或(pt)H2|OH-,(pt)O2|OH-或(pt)O2|H2O,H+及(pt)Cl2|Cl-来表示。其电极反应分别为:
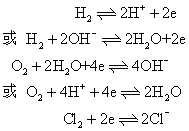
❷第二类电极 主要是微溶盐电极,由金属复盖一薄层该金属的一种微溶盐,然后浸入含该微溶盐负离子的溶液中构成。最常用的微溶盐电极是甘汞电极,用符号Hg-Hg2Cl2|Cl-表示。其电极反应为:
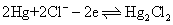
第二类电极在电化学中有较重要的意义,有许多负离子如SO2-4,C2O2-4等,没有对应的第一类电极,但可形成对应的第二类电极。另外一些负离子如Cl-和OH-,即使有对应的第一类电极,也常制成第二类电极,因后者比较容易制备,而且使用方便。
❸ 第三类电极 氧化还原电极,由惰性金属,如铂片,插入含有两种不同氧化态的同种离子溶液中构成。如Fe2+-Fe3+电极,用符号 (Pt) |Fe2+,Fe3+表示,电极反应为
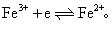
上述电极的充、放电电极反应都互为逆反应。用这样的两个电极组成电池,其充、放电电池反应必互为逆反应。若电池的工作方式符合热力学可逆过程的条件,便可成为可逆电池。
☚ 可逆电池 电极电势 ☛
- 刑事案件是什么意思
- 刑事案件办案期限是什么意思
- 刑事案件现场勘查规则是什么意思
- 刑事案件管辖是什么意思
- 刑事案例选编是什么意思
- 刑事检察是什么意思
- 刑事检察是什么意思
- 刑事法学大辞书是什么意思
- 刑事法学大辞书是什么意思
- 刑事法学大辞典是什么意思
- 刑事法学词典是什么意思
- 刑事法学词典是什么意思
- 刑事法律关系是什么意思
- 刑事测量是什么意思
- 刑事照相是什么意思
- 刑事照相是什么意思
- 刑事犯是什么意思
- 刑事犯罪现场是什么意思
- 刑事犯罪现场的保护是什么意思
- 刑事犯罪资料是什么意思
- 刑事现场勘查是什么意思
- 刑事现场照相是什么意思
- 刑事理化检验是什么意思
- 刑事申诉状是什么意思
- 刑事疑案研究是什么意思
- 刑事登记是什么意思
- 刑事登记是什么意思
- 刑事相貌学是什么意思
- 刑事社会学派是什么意思
- 刑事社会学派是什么意思
- 刑事科学技术是什么意思
- 刑事科学技术工作细则是什么意思
- 刑事立法是什么意思
- 刑事管辖权是什么意思
- 刑事管辖权是什么意思
- 刑事类推是什么意思
- 刑事类推是什么意思
- 刑事类推是什么意思
- 刑事自诉状是什么意思
- 刑事被告人是什么意思
- 刑事被告人心理是什么意思
- 刑事被害人学是什么意思
- 刑事裁判法律文书是什么意思
- 刑事裁定是什么意思
- 刑事裁定书是什么意思
- 刑事警察是什么意思
- 刑事访问的原理与方法是什么意思
- 刑事证据是什么意思
- 刑事证据学是什么意思
- 刑事证据理论研究综述是什么意思
- 刑事证据的理论与实践是什么意思
- 刑事诉讼是什么意思
- 刑事诉讼是什么意思
- 刑事诉讼是什么意思
- 刑事诉讼主体是什么意思
- 刑事诉讼主体是什么意思
- 刑事诉讼义务是什么意思
- 刑事诉讼任务是什么意思
- 刑事诉讼历史类型是什么意思
- 刑事诉讼原则是什么意思