1.与O2反应:
(1)常温下,Mg、Al均能与空气中的O2反应,生成一层坚固而致密的氧化物保护膜,所以金属镁和铝都有抗腐蚀性能.
(2)燃烧:

注 镁在空气中用酒精灯火焰点燃即可燃烧,而铝在空气中需高温点燃才能燃烧.这是由金属性Mg>Al所决定的,也是说明金属性Mg>Al的实例之一.
2.镁、铝除能跟氧气反应外,还能跟其他非金属如硫、卤素等起反应
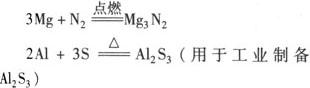
3.与酸反应
(1)与非氧化性酸反应:
如:Mg+2H+=Mg2++H2/p> 2Al+6H↑(+ (2)与氧化性酸反应: 如:4Mg+10HNO↓(3
铝在冷的浓HNO3、浓H2SO4中因发生钝化而难溶.
4.与碱反应:
(1)Mg与碱不反应
(2)Al与强碱溶液:
2Al+2NaOH+2H2O=2NaAlO2+3H2/p> 注 铝与强碱溶液反应机理为: 2Al+6H↓(2 Al(OH)↓(3
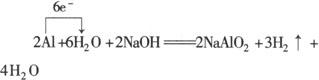
5.与水反应
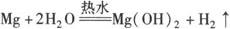
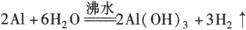
6.与氧化物反应:

注 铝热反应可用于焊接大截面金属(如铁轨)和冶炼某些难熔金属(如Mn、Cr等).
- 陈奉是什么意思
- 陈奉兹是什么意思
- 陈奉璋是什么意思
- 陈奎德是什么意思
- 陈奎生是什么意思
- 陈奕俭是什么意思
- 陈奕禧是什么意思
- 陈奕禧是什么意思
- 陈女是什么意思
- 陈好华是什么意思
- 陈好德是什么意思
- 陈如坤是什么意思
- 陈如本是什么意思
- 陈如松是什么意思
- 陈如泉是什么意思
- 陈如泉是什么意思
- 陈如馨是什么意思
- 陈妙常是什么意思
- 陈妙常是什么意思
- 陈妙恩是什么意思
- 陈妙玉是什么意思
- 陈妙珍是什么意思
- 陈姚最是什么意思
- 陈威是什么意思
- 陈威是什么意思
- 陈威是什么意思
- 陈威仁是什么意思
- 陈娟是什么意思
- 陈娟娟是什么意思
- 陈娟娟是什么意思
- 陈婉儿是什么意思
- 陈婉珍是什么意思
- 陈婉真是什么意思
- 陈婉贞是什么意思
- 陈婷婷是什么意思
- 陈子是什么意思
- 陈子云画册是什么意思
- 陈子伦是什么意思
- 陈子元是什么意思
- 陈子元是什么意思
- 陈子元是什么意思
- 陈子典是什么意思
- 陈子博是什么意思
- 陈子君是什么意思
- 陈子和是什么意思
- 陈子坚是什么意思
- 陈子奋是什么意思
- 陈子奋画集是什么意思
- 陈子奋白描花卉册是什么意思
- 陈子展是什么意思
- 陈子展是什么意思
- 陈子展是什么意思
- 陈子展是什么意思
- 陈子展是什么意思
- 陈子岐是什么意思
- 陈子干是什么意思
- 陈子庄是什么意思
- 陈子成是什么意思
- 陈子昂是什么意思
- 陈子昂是什么意思