酶反应动力学
酶反应动力学是指作用物浓度对单分子作用物酶反应速度的影响。实验结果表明作用物浓度[S]与反应速度(v)的关系是一条双曲线。
Michaelis—Menten曾对此作过数学分析,并导出所谓米氏方程及米氏常数。
将酶反应表示如下: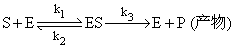
[E]t[S]t[ES]分别代表酶总浓度,作用物总浓度及酶作用物复体浓度,设[E]及[S]代表自由酶及自由作用物浓度,k1k2k3为各该反应的速度常数。
自由酶浓度[E]=[E]t-[ES]
自由作用物浓度[S]=[S]t-[ES] ∵[ES]很少
∴[S]=[S]t
E,S,ES到达平衡时,ES生成速度=ES解离速度
k1[E][S]=k2[ES]
[E]=[E]t-[ES]
∴k1([E]t-[ES])[S]=k2[ES]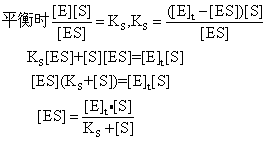 式中KS称为米氏常数实际上是ES的解离常数
式中KS称为米氏常数实际上是ES的解离常数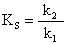
反应速度v=k3 [ES]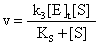 当所有的酶都成为ES时为最大速度Vmax
当所有的酶都成为ES时为最大速度Vmax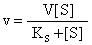
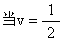 (即[ES]=[E]t时)
(即[ES]=[E]t时)
V时KS=[S],即达到半最大速度的KS值即为当时的[S]值。
Ks值愈小,ES生成愈速,解离愈慢,酶反应速度愈大。
以上依据化学平衡假设导衍米氏方程,该方程亦可依据稳态假设导衍之。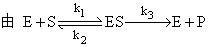
所谓稳态是指酶促反应中可以达到ES数量无改变,亦即ES生成速度=ES消失速度。
ES生成途径的速度是k1[E][S]
ES消失有两种途径:
❶ES解离成E及S,速度为K2[ES];
❷ ES转化为E及产物,速度为k3[ES]
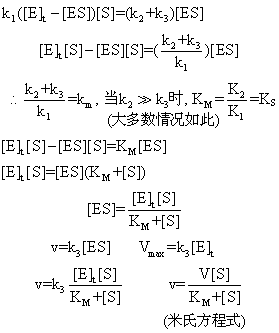
消失总速度=(k2+k3) [ES]
生成速度=消失速度 k1[E] [S]=(k2+k3) [ES]
KM值的用途 KM值在下列方面可能有实用意义。
(1)推测、鉴定不同个体,不同组织或同一个体的组织在不同发育期间催化同种化学反应的酶是否为同一种酶蛋白质。若在各情况下KM值均相同,则很可能是同一种酶,否则,可能是不同的酶。
(2) 估计细胞内代谢物的大致浓度范围。一般说来代谢物(酶的作用物的浓度是在它的KM值附近,从生理意义上推测,若[S]《KM,则酶反应速度对[S]改变太敏感,而且此时酶反应速度很小,浪费酶的催化能力。 若[S]》KM则酶反应速度对[S]太不敏感,从[S]同v的关系曲线上可见[S]增加几十倍,也只是将速度增到 [S]=KM时速度的两倍。这时通过代谢物浓度调节代谢速度的效率太低。
(3) 酶分子与某种物质结合可以改变它对作用物的KM近似值。若发现某酶在体外实验时KM值很大 [催化效果很低]可以启发去寻找细胞内有无物质能与酶结合而改变它的KM,使它能在细胞内更有效地发挥作用。也可能有相反的情况。
KS (KM)值的图解法 据米氏方程式
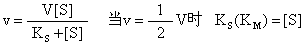 即当速度恰为半最大速度时,该时的[S]值即为KS (KM)值。将实验结果在v对[S]座标上做图得一条双曲线(见图)。由曲线上求出V值,在v=1/|V处找出相应[S]值即可。但此种方法往往因V值找不准确而出现误差。现有多种改良图解法可得较准确数值。例如Lineweaver—Burk采用双倒数法作图,即在1/v与1/[S]座标上作图,得一条直线。其依据是将米氏方程两端均取倒数,即得下式,在所得直线上可量出斜度及截矩、即可测量出KS(KM)值。
即当速度恰为半最大速度时,该时的[S]值即为KS (KM)值。将实验结果在v对[S]座标上做图得一条双曲线(见图)。由曲线上求出V值,在v=1/|V处找出相应[S]值即可。但此种方法往往因V值找不准确而出现误差。现有多种改良图解法可得较准确数值。例如Lineweaver—Burk采用双倒数法作图,即在1/v与1/[S]座标上作图,得一条直线。其依据是将米氏方程两端均取倒数,即得下式,在所得直线上可量出斜度及截矩、即可测量出KS(KM)值。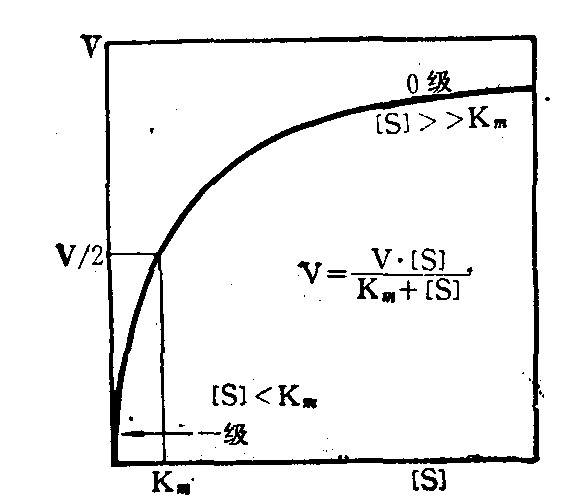
作用物浓度与反应速度关系图

此外尚有其它数种图解法。
酶浓度对反应速度的影响据米氏方程:
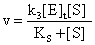 当S》KS时,可简化为
当S》KS时,可简化为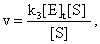 即此情况下速度与酶浓度成正比例。与[S]无关,[对作用物而言是零级反应]。当S
即此情况下速度与酶浓度成正比例。与[S]无关,[对作用物而言是零级反应]。当SpH对酶促反应的影响酶催化化学反应的能力显著地受pH的影响。酶一般是在中间pH值里具有最适的活性,在很高或很低pH时酶受破坏而活性降低。各种酶的最适pH值不同,pH的这种影响可能是由于下列两种一般性原因:
❶pH能影响酶的稳定性,使酶在最适pH的两远侧不可逆地丧失活性。在距最适pH不太远的部位酶活性的改变是可逆的,包括分子里某种基群的电离。
❷pH能影响酶促反应的动力学参数,也可能影响酶作用物复体的稳定性,pH还可能影响催化步骤的速度,或者说pH能对KM和Vmax都有影响。其中第二个一般原因似乎更有意义。因为动力学上量得出的常数KM和Vmax可能同化学键的生成及折断步骤有关。
温度对酶促反应速度的影响 几乎一切化学反应当温度升高时速度加快。温度T同反应速度常数k有下列经验关系:k=Ae-(Ea/RT)(Arrhenius方程式)
式中k为速度常数,Ea为活化能。R、A为常数,Ea和A都不受温度影响。T为绝对温度。
温度对酶促反应速度的影响包括:
❶温度对反应速度的一般影响,温度增加。使反应加速。
❷温度对酶破坏速度的影响(温度增加,使酶的破坏加速)结果使反应减慢。但有一种温度能使上述两影响调和到最佳点即能有一个速度最大的温度。此种温度称为酶的最适温度。人体内的最适温度在38℃左右。
- 驻斾是什么意思
- 驻旌是什么意思
- 驻日是什么意思
- 驻春是什么意思
- 驻春园小史是什么意思
- 驻春堂是什么意思
- 驻景是什么意思
- 驻景丸是什么意思
- 驻景亭是什么意思
- 驻景挥戈是什么意思
- 驻景补肾明目丸是什么意思
- 驻月是什么意思
- 驻有军事指挥部的军营是什么意思
- 驻有军警的关卡是什么意思
- 驻极体是什么意思
- 驻欧美军总部是什么意思
- 驻止是什么意思
- 驻止之敌是什么意思
- 驻步是什么意思
- 驻毂是什么意思
- 驻气是什么意思
- 驻泊是什么意思
- 驻泊兵马钤辖是什么意思
- 驻泊医官是什么意思
- 驻泊厅是什么意思
- 驻泊巡检是什么意思
- 驻泊都监是什么意思
- 驻泊都部署是什么意思
- 驻波是什么意思
- 驻津机构经贸区是什么意思
- 驻津英国总领事署旧址是什么意思
- 驻浮云是什么意思
- 驻港理货是什么意思
- 驻港英军是什么意思
- 驻港部队是什么意思
- 驻湘军事院校是什么意思
- 驻澳门特别行政区领事馆是什么意思
- 驻点是什么意思
- 驻牙是什么意思
- 驻甘八旗兵是什么意思
- 驻留是什么意思
- 驻留轨道是什么意思
- 驻留轨道上惯性飞行是什么意思
- 驻疑是什么意思
- 驻白日是什么意思
- 驻盖是什么意思
- 驻目是什么意思
- 驻眼是什么意思
- 驻立是什么意思
- 驻笔是什么意思
- 驻粤八旗志是什么意思
- 驻綍是什么意思
- 驻綍辞清庙,凝笳背直城。是什么意思
- 驻红却白是什么意思
- 驻罕是什么意思
- 驻耳是什么意思
- 驻联合国代表是什么意思
- 驻联合国代表团是什么意思
- 驻脚是什么意思
- 驻色是什么意思