相对原子质量
相对原子质量xiangdui yuanzi zhiliang
旧称原子量。19世纪初J.道尔顿在提出原子学说的同时就提出了原子量概念。他将氢原子量定为1.0,并以此做标准,根据物质质量组成及假定其中原子个数比,如把水中氢和氧原子个数比定为1: 1,然后对比得出其他元素原子量。1803年他发表了世界上第一张原子量表。因为氧的化合物比氢的化合物多,1818年J.J.贝采利乌斯将氧原子量定为100,并以此做基准。1860年J.S.斯塔提出将天然氧定为16,并以此做基准,这样既照顾了化学法测定的方便,又能使最轻氢元素的原子量约等于1,因此这个基准一直沿用下来。1929年发现氧有3种核素,即O16,O17,O18。后来又证实氧同位素不是均匀地分布于自然界。用天然氧做原子量标准不够完善,物理界改用O16等于16做标准,化学界仍采用天然氧等于16做基准。当用物理标准时,氧的各种同位素原子量分别为:O16等于16.0000,O17等于17.0045,O18等于18.0049。因此,自然界中,氧平均原子量为16. 0044,两 者 比 值 16. 0044/16.0000=1.000275。
1940年国际原子量委员会 (ICAW) 开始采用1.000275为两种标准的换算因数,即
物理原子量=1.000275×化学原子量
1959年马托赫向国际化学协会建议以12C等于12为原子量新基准,可使各元素原子量变动不大。因为12C在碳的天然同位素中所占相对百分数比较固定,而且质谱法测定12C的质量也较精确。1960年和1961年国际物理学会和化学会分别接受了这个建议。从此原子量有了统一的新基准,不再存在所谓化学原子量和物理原子量的区别,而统一改称为国际原子量。
1979年国际原子量委员会提出新定义,一种元素的原子量是“该元素1 mol质量对核素12C 1 mol质量1/12的比值”。即,原子量的真实涵义是元素的相对原子质量,是元素的平均原子质量与核素12C原子质量的1/12之比。元素的平均原子质量是元素各核素的原子质量与其百分含量 (丰度) 乘积的加合。
1973年国际计量局公布了原子质量的单位为u; 而核素12C原子质量为12u。
1u=1.660 57×10-27 kg
求元素相对原子质量 (Ar) 的公式为:
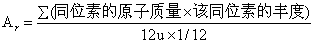
可见,相对原子质量是无量钢的,是相对的比值; 而原子质量是有单位的,是绝对值。一种元素相对原子质量只有一个,而多核素却有多个原子质量。相对原子质量与核素的丰度有关; 而原子质量与核素的丰度无关。地球上元素的天然同位素分布并非恒定,元素相对原子质量并不是自然界的 一种常数,ICAW根据地球上天然来源试样的测定结果,一般每两年公布一次新的国际原子量表。
测定相对原子质量的方法有多种,如用元素的当量、固体的比热以及物质的分子量来测定相对原子质量。这些方法所使用的实验设备比较简单,因而测定准确度也不够高。1919年英国的F.W.阿斯顿,改进了W.汤姆逊的磁分离器,制成了世界上第一台质谱仪,从而开始了测定相对原子质量的现代方法——质谱法。质谱仪不仅能测出元素的相对原子质量,还能反映出不同质量的原子所占的百分比。
☚ 原子序数 原子量 ☛
- 火飘飘是什么意思
- 火飛抓是什么意思
- 火飞抓是什么意思
- 火食是什么意思
- 火食堂子是什么意思
- 火食天是什么意思
- 火食瘤是什么意思
- 火食码子是什么意思
- 火香是什么意思
- 火马冲镇是什么意思
- 火马郎是什么意思
- 火驰是什么意思
- 火验是什么意思
- 火骨是什么意思
- 火高有三千丈是什么意思
- 火魚是什么意思
- 火鱼是什么意思
- 火鲁刺思部是什么意思
- 火鲁剌思是什么意思
- 火鲁火孙是什么意思
- 火鲁火疃是什么意思
- 火鲁火疃谋克是什么意思
- 火鴉是什么意思
- 火鸟是什么意思
- 火鸟祥禽是什么意思
- 火鸠是什么意思
- 火鸡是什么意思
- 火鸡比天鹅是什么意思
- 火鸡球虫病是什么意思
- 火鸡雏是什么意思
- 火鸡面是什么意思
- 火鸡黑冠病是什么意思
- 火鸡(吐绶鸡)是什么意思
- 火鸣菜是什么意思
- 火鸦是什么意思
- 火鹞是什么意思
- 火麦是什么意思
- 火麻是什么意思
- 火麻仁是什么意思
- 火麻子是什么意思
- 火麻布是什么意思
- 火麻棱是什么意思
- 火黄是什么意思
- 火鼎是什么意思
- 火鼓是什么意思
- 火鼠是什么意思
- 火鼠布是什么意思
- 火鼠论寒,冰蚕语热,定谁同异。是什么意思
- 火齊是什么意思
- 火齊珠是什么意思
- 火齊鏡是什么意思
- 火齌是什么意思
- 火齐是什么意思
- 火齐指环是什么意思
- 火齐木难是什么意思
- 火齐珠是什么意思
- 火齐镜是什么意思
- 火龍是什么意思
- 火龍出水是什么意思
- 火龍捲地飛車是什么意思