电化学分析法electrochemical analysis
建立在溶液电化学性质上的一类化学分析方法。溶液的电化学现象一般发生在化学电池中。化学电池主要包括电解质溶液和放置于其中的两个电极。溶液的电化学性质(如电极电位、电流、电导、电量等)与化学性质(电解质溶液的化学组成、浓度、氧化态与还原态的比率等)之间存在着一定的关系,电化学分析法就是利用这些关系,通过电极这个变换器,把被测物质的浓度转化成电学参数而加以测量的分析方法。
根据国际纯粹化学与应用化学联合会倡议,电化学分析法分为3类:❶不涉及双电层和电极反应。包括电导分析法、高频滴定法等。
❷涉及双电层。但不涉及电极反应。例如通过测量表面张力或法拉第阻抗而测定浓度的分析方法。
❸涉及电极反应。包括电位分析法、电解分析法、库仑分析法、极谱分析法和伏安法等。
电化学分析法是仪器分析中普遍应用的一类方法,这类方法具有快速、灵敏、准确和适用面广的特点,由于在测量过程中得到的是电学讯号,因而易于实现自动化和连续分析。农业化学分析中已被普遍采用。
电化学分析法
仪器分析法的一种。是基于被分析溶液的各种电化学性质来确定其组成和含量的 一类分析方法。主要包括电位分析法、极谱分析法、电重量分析和电解分析法、库仑分析法、电导分析法等。
电化学分析法
电化学分析法是基于被分析溶液的各种电化学性质来确定其组成及含量的分析方法。主要包括电位分析法、极谱分析法、电重量分析法和电解分离法、库仑分析法、电导分析法等。本条主要介绍生物医学中广泛应用的电位分析法,并对其他电化学法作一简单介绍。
基本原理
电极电位 与金属组成的电极上有如下的电极反应: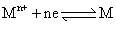 它们的电极电位遵守Nernst方程:
它们的电极电位遵守Nernst方程: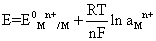 其中,E0Mn+/M—标准电极电位,R—气体常数,T—绝对温度,F—法拉第常数(25℃,RT/F=0.059),aMn+—Mn+的活度,可用[Mn+]近似地代替。
其中,E0Mn+/M—标准电极电位,R—气体常数,T—绝对温度,F—法拉第常数(25℃,RT/F=0.059),aMn+—Mn+的活度,可用[Mn+]近似地代替。
根据上式可见电极电位能反映出溶液中金属离子的浓度(活度)。因此,这些金属电极可以指示相应金属离子的浓度,故名指示电极。常用的指示电极有银、汞等电极。
氧化还原半电池反应: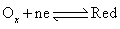 的电位可以由铂、金等贵金属指示出来,其电极电位为:
的电位可以由铂、金等贵金属指示出来,其电极电位为: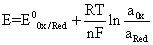 或近似地写为:
或近似地写为:![]() 因此,铂、金等贵重金属电极常用作氧化还原电位的指示电极,可用以测定[Ox]/[Red]比值的大小。
因此,铂、金等贵重金属电极常用作氧化还原电位的指示电极,可用以测定[Ox]/[Red]比值的大小。
另外还有一类指示电极是由金属、其难溶盐及相应的阴离子组成,如Ag—AgCl,Hg—Hg2Cl2等电极。半电池反应为: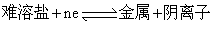 例如:
例如: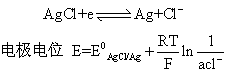 以Ag—AgCl电极为例说明指示电极工作原理:按Nernst方程,银电极的电极电位:
以Ag—AgCl电极为例说明指示电极工作原理:按Nernst方程,银电极的电极电位: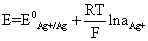 在Ag—AgCl电极中,与银接触的银离子由AgCl解离出来,其活度取决于AgCl的活度常数和溶液中Cl-活度。
在Ag—AgCl电极中,与银接触的银离子由AgCl解离出来,其活度取决于AgCl的活度常数和溶液中Cl-活度。
aAg+×ac1-=KSP(Agc1)
aAg+=KSP/ac1-代入银电极电位公式得:
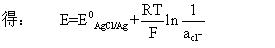 因此这类电极可以用来指示阴离子活度的变化。
因此这类电极可以用来指示阴离子活度的变化。指示电极应符合下列基本要求:
❶电极电位与有关离子浓度(准确地说应该是活度)之间应该符合Nernst方程;
❷对有关离子浓度的变化,响应快且能够重现;
❸便于使用。
电极电位的测量和参比电极 单一电极的电位无法测量,必须把它和另一个电极连在一起形成一个电池,用电位计测定这个电池的电动势 (E.M.F.),只要另一个电极的电位恒定并已经知道,根据下面关系,就能求出欲测电极的电位。
E.M.F.=E+-E-
式中E+代表电位较高那一极的电极电位,E-代表电位较低那一极的电极电位。电位值已知的电极叫做参比电极。最早的参比电极为标准氢电极,它是以1大气压纯氢饱和的镀有铂黑的铂片与H+活度为1的盐酸所组成,其电极反应为:
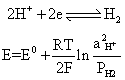 因为氢气的压力(PH2)及氢离子活度都是固定的 (1大气压及1mol),所以电极电位也是固定的,作为氢电极的标准电极电位,被人为地定为零(在任何温度下)。这种电极装配麻烦,在日常工作中很少应用。通常用饱和甘汞电极等作为参比电极,它们的电极电位已知与标准氢电极比较,并精密地测定过。
因为氢气的压力(PH2)及氢离子活度都是固定的 (1大气压及1mol),所以电极电位也是固定的,作为氢电极的标准电极电位,被人为地定为零(在任何温度下)。这种电极装配麻烦,在日常工作中很少应用。通常用饱和甘汞电极等作为参比电极,它们的电极电位已知与标准氢电极比较,并精密地测定过。参比电极应符合下列的基本要求:
❶可逆性好,即测量电动势过程中,当有微弱电流通过时,电极电位保持不变。
❷重现性好,这是指电极能依照Nernst方程式而对温度或浓度的改变无滞后现象,能建立一种可行的制备电极的标准方程; 用这种方法制备的电极电位恒定。
❸稳定性好,使用寿命长。
测量电池电动势时只允许没有或仅有微弱的电流通过,否则测量结果就会有偏差。这有两方面的原因,其一是当通过电池电流较大时,由于电极反应,电极附近有关离子浓度发生变化,使电极电位改变,致使测得的电动势低于应有的数值,这种现象称为浓差极化。另一方面由于电池存在内阻,通过电流后就会产生IR电位降(I电流,R电阻),测得电动势值为(E.M.F.-IR)。这项误差在电池内阻较大的情况下尤其要注意。
氢离子选择性电极及溶液pH的测定
氢电极 电极反应为:
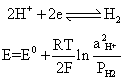 E0=0,维持PH2=1 (大气压),则
E0=0,维持PH2=1 (大气压),则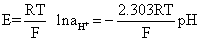 氢电极响应范围广(pH1~14),结果准确,误差为±0.01pH。但应用受到下列条件的限制——氢气要求很纯; 必须准确测知其压力; 溶液中不能有氧化剂及还原剂或不饱和的有机化合物。蛋白质和胶体物质易为铂黑所吸附,也会使电极反应不灵敏、不稳定等。只有在精密测定中才用它。
氢电极响应范围广(pH1~14),结果准确,误差为±0.01pH。但应用受到下列条件的限制——氢气要求很纯; 必须准确测知其压力; 溶液中不能有氧化剂及还原剂或不饱和的有机化合物。蛋白质和胶体物质易为铂黑所吸附,也会使电极反应不灵敏、不稳定等。只有在精密测定中才用它。玻璃电极 是测定pH最常用的指示电极。它是在一支玻璃管下端接上一个特殊质料的玻璃球形薄膜,内盛一定pH值的缓冲溶液,并含有一定浓度的氯化钾,浸入一支银-氯化银电极或甘汞电极作为内参比电极而成。玻璃电极能指示pH变化,主要是由于玻璃膜的作用,其组分一般为22%Na2O、6%CaO、72%SiO2。这种玻璃的结构是由固定的带负电的硅酸晶格组成。在晶格中,存在较小的但活动能力较强的正离子,主要是钠离子。溶液中的氢离子能进入硅酸晶格代替Na+的位点,但其他负离子却被带负电的硅酸晶格所排斥。二价和高价的正离子也不能进出硅酸晶格。当玻璃膜泡在水中时,由于硅酸结构与H+所结合的键的强度远大于与Na+的强度(约104倍),因此发生如下的离子交换反应:
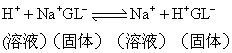 反应的平衡常数很大,有利于正反应,使得玻璃膜表面的点位在酸性和中性时,几乎全为H+所占据而形成一个硅酸(H+GL-)水化层 (水合玻璃层)。由于玻璃电极的内室盛有一定pH的缓冲液,因此,在玻璃膜内侧还有一水合玻璃层。插入到待测液中即成:
反应的平衡常数很大,有利于正反应,使得玻璃膜表面的点位在酸性和中性时,几乎全为H+所占据而形成一个硅酸(H+GL-)水化层 (水合玻璃层)。由于玻璃电极的内室盛有一定pH的缓冲液,因此,在玻璃膜内侧还有一水合玻璃层。插入到待测液中即成:待测液|水合玻璃层|干玻璃层|水合玻璃层|内部溶液当待测液中H+高于水合玻璃层,则扩散进入水合玻璃层,由于其它阴离子不能进入,所以产生电位差(溶液带负电,水合玻璃层带正电); 当待测液中H+低于水合玻璃层时,则水合玻璃层的H+进入溶液产生电位差(溶液带正电,水合玻璃层带负电)。电位差达一定值后,H+的出入相等,成平衡状态。这时膜内外两个界面的电位值分别为:
 一般来说,假设玻璃膜内外表面的结构状态一致,则H+在两个表面可能交换Na+占据的位点数目也是一致的,那么K1=K2,aH+(水合玻璃层)内=aH+(水合玻璃层)外,膜电位
一般来说,假设玻璃膜内外表面的结构状态一致,则H+在两个表面可能交换Na+占据的位点数目也是一致的,那么K1=K2,aH+(水合玻璃层)内=aH+(水合玻璃层)外,膜电位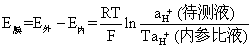
因为内参比液pH一定,所以
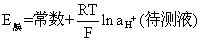
pH玻璃电极是一种对氢离子具有高度选择性的指示电极,不受氧化剂、还原剂的影响,可用于有色、浑浊或胶态溶液的pH测定。操作简便,达平衡快,不沾污试液。但使用前要在纯水中浸泡24小时以上,且不能用于含氟离子的溶液。
pH玻璃电极对pH的响应也有一定的范围 (1~10),pH很低产生酸误差,测得pH值比实际值高,原因不明。pH很高则产生碱误差,测得pH值较实际低,这是因为在强碱液中,H+浓度低,碱金属离子如Na+也会在玻璃膜上交换而产生电位响应,钠离子的响应最明显,有时又称为钠误差。国产221型pH玻璃电极即属此类。锂玻璃膜的玻璃电极,虽然溶液pH高达14也无钠误差。国产231型pH玻璃电极即属此类。
离子选择电极
pM响应电极 改变玻璃膜的组分可以得到对各种金属离子响应的玻璃电极。 如15%Li2O、25%Al2O
 60%SiO2的玻璃电极可测定Li+; 11%Na2O、18%Al2O3、71%SiO2可测Na+; 27%Na2O、5%Al2O3、68%SiO2可测K+; 11%Na2O、15%Al2O3、71%SiO2可测Ag+。它们的原理类似于pH玻璃电极。
60%SiO2的玻璃电极可测定Li+; 11%Na2O、18%Al2O3、71%SiO2可测Na+; 27%Na2O、5%Al2O3、68%SiO2可测K+; 11%Na2O、15%Al2O3、71%SiO2可测Ag+。它们的原理类似于pH玻璃电极。固态膜选择电极 用单晶体或把晶体沉淀压成薄片后,可以制成固态膜电极。用得最广泛的是氟离子选择电极。其薄膜是用纯的或掺杂3Eu3+(增加导电性) 的LaF3单晶作原料。用AgCl、AgBr、AgI、Ag2S等晶态沉淀压成薄片后,也可以制成结构与氟离子选择电极相似的固态膜电极,相应地可测定Cl-、Br-、I-、CN-和S2-等离子的活度。
固态膜的膜电位的产生与玻璃膜相似。在氟化镧(LaF3)晶体中,离子传导过程是由F-实现的。因此膜电位产生是由于F-进出LaF3晶格的结果。OH-的大小和电荷与F-相似,也能进出LaF3晶格,因此对氟电极有响应。为了消除OH-的干扰,测定F-时通常控制溶液pH值为5.5~6.5。
固态膜选择电极的选择性一般较高。干扰通常不是由于外来离子进入晶格所引起,而是在电极表面上发生的化学反应所致。例如对Cl-选择电极(由AgCl组成),能与Ag+生成难溶盐的阴离子,象I-、Br-、S2-,严重干扰Cl-的测定,这是由于AgBr和AgI的溶度积远小于AgCl之故。反过来,Cl-对I-、Br-等选择电极无影响。
液态膜离子选择性电极 某些液体离子交换剂难溶于水,而对某阳离子或阴离子的结合具有选择性。将已为被测离子交换过的液体离子交换剂溶解于憎水性的有机溶剂之中,然后把它置在多孔性膜内,构成一个液态膜。这个膜与水溶液之间形成相界面。待测离子进出这层膜形成电位差。
液态膜离子选择性电极的选择性一般不如固态膜电极,原因是较高的离子能出入有机相与液体交换剂进行交换。
目前已发展出能够测量细胞内液离子活度的微型液态膜电极。
酶电极 尿素酶使溶液中的尿素转化为铵离子,含酶的凝胶层包围在铵离子选择电极周围,产生出来的NH4+通过扩散到达电极表面,由电位给出尿素的浓度。由酪氨酸脱羧酶凝胶层与二氧化碳电极耦合,可以做成高选择性1-酪氨酸电极。将掺有青霉素酶的聚丙烯薄凝胶膜塑在氢离子玻璃电极周围,设计成青霉素选择电极,能检测青霉素水解为青霉素酸时增加的酸度。
酶的专一性赋于电极很高的选择性。
其他选择电极 已经发展出一些气敏电极,可响应氨、胺类、二氧化硫、二氧化氮、硫化氢、氰化氢、醋酸或氯气。
其他电化学分析方法简介
极谱分析法 是在特殊条件下进行的电解分析。它是用滴汞电极来电解被分析物质的稀溶液,并根据得到的电压-电流曲线来进行分析的方法。适合于测定物质浓度范围为10-5~10-2mol,相对误差约为2~5%。
电导分析法 是将分析溶液放在由固定面积、固定距离的两个铂电极所构成的电导池中,通过测量溶液的电导(或电阻)来确定被测物质的含量。电导分析法的原理是基于溶液的电导 (电阻的倒数) 与存在于溶液中各离子的浓度、运动速度和电荷数有关。水的纯度和天然水的盐度等的测定常用电导法。电导法还可与分离方法(如高效液层析) 联合使用,作为分离过程的一种鉴定器。
电重量分析法及电解电离法 电重量分析法是应用电解作用进行分析的一种方法,即通过电解使待测物质在已知重量的电极上析出,从而得出其含量。电解作用也可应用于金属离子的分离,因为各种金属离子具有不同的析示电位。
库仑分析法 是通过测定被分离物质定量地进行某一电极反应,或者它与某一电极反应的产物定鼠地进行化学反应所消耗的电量 (库仑数) 来进行定量分析的方法。
电化学分析法
电化学分析法是根据被测定物质的电化学性质进行分析的一类方法。可以测量在该物质的溶液中两电极间的电流、电位或电阻,由其绝对数值求出物质含量或由这些数值的变化而确定滴定的终点。
常用的电化学分析方法有电位滴定法、电导滴定法、安培滴定法、库伦分析法、极谱分析法等。
- 成也萧何,败也萧何是什么意思
- 成也萧何,败也萧何是什么意思
- 成也萧何,败也萧何是什么意思
- 成也萧何,败也萧何是什么意思
- 成也萧何,败也萧何是什么意思
- 成事不说,既往不咎是什么意思
- 成事不足,坏事有余是什么意思
- 成事不足,败事有余是什么意思
- 成事不足,败事有余是什么意思
- 成事不足,败事有余是什么意思
- 成事在人是什么意思
- 成于乐是什么意思
- 成井工艺是什么意思
- 成交是什么意思
- 成交价格是什么意思
- 成交价格是什么意思
- 成交价格是什么意思
- 成交数量是什么意思
- 成交样品是什么意思
- 成交股数与成交额是什么意思
- 成交量比率指标是什么意思
- 成人是什么意思
- 成人是什么意思
- 成人不自在,自在不成人是什么意思
- 成人不自在,自在不成人是什么意思
- 成人不自在,自在不成人是什么意思
- 成人之恶是什么意思
- 成人之美是什么意思
- 成人之美是什么意思
- 成人之美是什么意思
- 成人之美是什么意思
- 成人之美是什么意思
- 成人人格发展是什么意思
- 成人体育与保健是什么意思
- 成人依恋是什么意思
- 成人内外控量表是什么意思
- 成人型呼吸窘迫综合征是什么意思
- 成人型呼吸窘迫综合征是什么意思
- 成人学习心理与教学是什么意思
- 成人学习资助试点工作实施是什么意思
- 成人学校休学、复学管理是什么意思
- 成人学校兴起是什么意思
- 成人感是什么意思
- 成人护理专修科教材是什么意思
- 成人教育是什么意思
- 成人教育是什么意思
- 成人教育是什么意思
- 成人教育是什么意思
- 成人教育是什么意思
- 成人教育是什么意思
- 成人教育是什么意思
- 成人教育是什么意思
- 成人教育是什么意思
- 成人教育是什么意思
- 成人教育是什么意思
- 成人教育是什么意思
- 成人教育是什么意思
- 成人教育制度是什么意思
- 成人教育协调指导工作委员会是什么意思
- 成人教育基础是什么意思