王水的氧化性
王水的氧化性wangshui de yanghuaxing
浓硝酸与浓盐酸的混合物 (摩尔比1:3) 称为王水,它的氧化能力极强,可溶解金、铂等金属:
Au+HNO3+4HCl=HAuCl4+NO↑+2H2O
3Pt+4HNO3+18HCl
=3H2[PtCl6]+4NO↑+8H2O
❶王水中的硝酸和盐酸发生反应,生成了比浓硝酸氧化性强的氯化亚硝酰 (还有氯气) :
HNO3+3HCl=NOCl+Cl2+2H2O
王水中氯离子的浓度很大,它能与金离子、铂离子形成稳定配离子([AuCl4]-,[PtCl6]2-) ,使金和铂的标准电极电势降低,从而使反应向金属溶解的方向进行。例如:
Au3++3e=Au 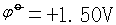
AuCl4+3e=Au+4Cl- 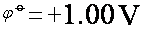
☚ 硝酸的氧化性 不同物质中同种元素间的氧化-还原反应 ☛
- 1k1h【一唱一和】是什么意思
- 1k1k【一吟一咏】是什么意思
- 1k1r【感恩戴德】是什么意思
- 1k1s【有口皆碑】是什么意思
- 1k1t【大吹大擂】是什么意思
- 1k1y【一呼百诺】是什么意思
- 1k22【甚嚣尘上】是什么意思
- 1k2k【龙吟虎啸】是什么意思
- 1k2t【迂回曲折】是什么意思
- 1k33【七嘴八舌】是什么意思
- 1k3h【一叶知秋】是什么意思
- 1k4r【不逞之徒】是什么意思
- 1k53【有口难分】是什么意思
- 1k54【声嘶力竭】是什么意思
- 1kcm【一叶蔽目】是什么意思
- 1kh3【一团和气】是什么意思
- 1khh【不吃烟火食】是什么意思
- 1kk3【素口骂人】是什么意思
- 1kkt【感恩图报】是什么意思
- 1kr1【大器晚成】是什么意思
- 1ktm【两叶掩目】是什么意思
- 1kx3【一鸣惊人】是什么意思
- 1m11【否极泰来】是什么意思
- 1m13 【有机可乘】是什么意思
- 1m14【耳目一新】是什么意思
- 1m1c【无根无蒂】是什么意思
- 1m1h【过眼云烟】是什么意思
- 1m1k【丧权辱国】是什么意思
- 1m1m【不闻不问】是什么意思
- 1m1n【百闻不如一见】是什么意思
- 1m1r【盛极一时】是什么意思
- 1m1w【有眼无珠】是什么意思
- 1m1x【面目可憎,语言无味】是什么意思
- 1m1y【过目成诵】是什么意思
- 1m1z【不骄不躁】是什么意思
- 1m1【下马威】是什么意思
- 1m21【不相上下】是什么意思
- 1m22【龙骧虎步】是什么意思
- 1m23【一马当先】是什么意思
- 1m24【龙骧虎视】是什么意思
- 1m2m【南枝北枝】是什么意思
- 1m2r【死马当作活马医】是什么意思
- 1m2s【开门见山】是什么意思
- 1m31 【二桃杀三士】是什么意思
- 1m32【面目全非】是什么意思
- 1m33 【唇枪舌剑】是什么意思
- 1m34【十目所视,十手所指】是什么意思
- 1m35【五马分尸】是什么意思
- 1m3m【车马盈门】是什么意思
- 1m43【残杯冷炙】是什么意思
- 1m44【龙马精神】是什么意思
- 1m4c【犬马之劳】是什么意思
- 1m4k【万马齐喑】是什么意思
- 1m53【大材小用】是什么意思
- 1m5y【博闻强记】是什么意思
- 1mc1【春树暮云】是什么意思
- 1mc2【有目共赏】是什么意思
- 1mcm【有目共睹】是什么意思
- 1mcs【一枕黄粱】是什么意思
- 1mmm【不相闻问】是什么意思