溶液的pH
溶液的pHrongye de pH
pH是表示溶液中氢离子浓度的一种方法。pH代表氢离子浓度的负对数,即 pH=-lg [H+]
例如,0.001 mol· L-1 盐酸溶液的 pH值为-lg0.001=3。pH值与 [H+] 的关系是pH值越小,[H+] 越大,酸度越高; pH值越大,[H+] 越小,酸度越低。pH值减小一个单位相当于 [H+] 增大10倍,pH值增大一个单位相当于 [H+] 减小至原来的1/10。中性溶液的pH是7,酸性溶液的pH小于7,碱性溶液的pH大于7。
同样,[OH-]也可用pOH表示: pOH=-lg[OH-],因[H+][OH-]=KW=10-14,两边取对数得:
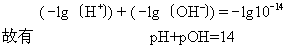
[H+],[OH-],pH,pOH的关系
| [H+] | [OH-] | pH | pOH | 溶液 |
| 10°=1 10-1 10-2 | 10-14 10-13 10-12 | 0 1 2 | 14 13 12 | 强酸性 |
| 10-3 10-4 10-5 10-6 | 10-11 10-10 10-9 10-8 | 3 4 5 6 | 11 10 9 8 | 酸性增强 |
| 10-7 10-8 10-9 | 10-7 10-6 10-5 | 7 8 9 | 7 6 5 | 中性 |
| 10-10 10-11 10-12 | 10-4 10-3 10-2 | 10 11 12 | 4 3 2 | 碱性增强 |
| 10-13 10-14 | 10-1 10°=1 | 13 14 | 1 0 | 强碱性 |
☚ 水的离子积 离子强度 ☛
- учреждéние-дóнор是什么意思
- учёт是什么意思
- учётчик是什么意思
- ущéрб是什么意思
- уэп(упр
 вление по борьбé с эконом
вление по борьбé с эконом ческими преступлéниями)是什么意思
ческими преступлéниями)是什么意思 - ф是什么意思
- ф
 брика是什么意思
брика是什么意思 - ф
 за是什么意思
за是什么意思 - ф
 ктор是什么意思
ктор是什么意思 - ф
 кторинг(英factoring)是什么意思
кторинг(英factoring)是什么意思 - ф
 льшь是什么意思
льшь是什么意思 - ф
 стинг(英fasting)是什么意思
стинг(英fasting)是什么意思 - ф
 рма是什么意思
рма是什么意思 - ф
 рма-агéнт是什么意思
рма-агéнт是什么意思 - ф
 рма-аренд
рма-аренд тор是什么意思
тор是什么意思 - ф
 рма-арендов
рма-арендов тель是什么意思
тель是什么意思 - ф
 рма-аукцион
рма-аукцион тор是什么意思
тор是什么意思 - ф
 рма-гиг
рма-гиг нт是什么意思
нт是什么意思 - ф
 рма-изготов
рма-изготов тель是什么意思
тель是什么意思 - ф
 рма-конкурéнт是什么意思
рма-конкурéнт是什么意思 - ф
 рма-контрагéнт是什么意思
рма-контрагéнт是什么意思 - ф
 рма-л
рма-л дер是什么意思
дер是什么意思 - ф
 рма-лицензи
рма-лицензи р是什么意思
р是什么意思 - ф
 рма-лицензи
рма-лицензи т是什么意思
т是什么意思 - ф
 рма-офферéнт是什么意思
рма-офферéнт是什么意思 - ф
 рма-подрядчик是什么意思
рма-подрядчик是什么意思 - ф
 рма-посрéдник是什么意思
рма-посрéдник是什么意思 - ф
 рма-поставщ
рма-поставщ к是什么意思
к是什么意思 - ф
 рма-продавéц是什么意思
рма-продавéц是什么意思 - ф
 рма-продуцéнт是什么意思
рма-продуцéнт是什么意思 - ф
 рма-ри
рма-ри лтер是什么意思
лтер是什么意思 - ф
 рма-спóнсор是什么意思
рма-спóнсор是什么意思 - ф
 рма-сток
рма-сток ст是什么意思
ст是什么意思 - ф
 рма-уч
рма-уч стник是什么意思
стник是什么意思 - ф
 рма-учред
рма-учред тель是什么意思
тель是什么意思 - ф
 рма-экспонéнт是什么意思
рма-экспонéнт是什么意思 - ф
 рма-экспортёр是什么意思
рма-экспортёр是什么意思 - ф
 шинг(英phishing)是什么意思
шинг(英phishing)是什么意思 - ф
 шка是什么意思
шка是什么意思 - фéрма是什么意思
- фéрмер是什么意思
- фéрмерство是什么意思
- фóлио是什么意思
- фóндовец是什么意思
- фóрвард-курс是什么意思
- фóрвард-р
 нок是什么意思
нок是什么意思 - фóрвард(英forward)是什么意思
- фóринт是什么意思
- фóрма是什么意思
- фóрмула是什么意思
- фóрчун(英fortune)是什么意思
- фóсстис是什么意思
- фýзия是什么意思
- фýнкция是什么意思
- фабержé是什么意思
- фабрик
 нт是什么意思
нт是什么意思 - фабрик
 т是什么意思
т是什么意思 - фабрик
 ция是什么意思
ция是什么意思 - фавор
 т是什么意思
т是什么意思 - фаворит
 зм是什么意思
зм是什么意思