求中和热
求中和热qiu zhonghere
酸碱中和反应是放热反应,在稀溶液中(1mol·L-1以下),1摩尔H+和1摩尔OH-发生中和反应而生成1摩尔水的反应热,就是中和热。中和热是一个定值——57.3kJ·mol-1。
H++OH-=H2O △Hm=57.3kJ·mol-1
有二元强酸参加的中和反应,酸的二步电离需吸收热量; 弱酸跟弱碱中和,分子电离成离子要吸收热量,放出的热量要少,测出的中和热数值偏低。
例1 含有10g Ba(OH)2的溶液跟适量硫酸反应,放热Q=6.646kJ,求该反应的中和热。
解 10g Ba(OH)2中含OH-的物质的量n(OH-)=10/171×2 mol,生成1mol H2O时放热:
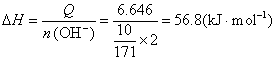
答 该反应的中和热为56.8 kJ·mol-1。
通过测定反应前后溶液温度的变化,可利用下式确定中和反应放出的热量:
Q=c·m·△t
式中 c——比热容 (J·g-1·K-1或kJ·kg-1·K-1)
m——溶液的质量(g或kg)
△t——溶液的温度升高量(K或℃)
水及稀溶液密度ρ=1g·mL-3;比热c=4.18 J·g-1·K-。
例2 根据表中数据,求中和热。
| 实验 次数 | HCl溶液 | NaOH溶液 | 溶液温度 | |||
| 浓度/ mol ·L-1 | 体积/ mL | 浓度/ mol·L-1 | 体积/ mL | 混合前/ t1 | 混合后/ t2 | |
| Ⅰ | 2 | 100 | 2 | 100 | 20 | 33.6 |
| Ⅱ | 1 | 150 | 1 | 150 | 20 | 26.8 |
解
❶根据实验Ⅰ数据:
Q=c·m·△t=4.18×(100+100)×(33.6-20)≈11.37(kJ)
依题意: (2×0.1)mol的HCl和NaOH中和生成(2×0.1)mol水时放出11.37kJ的热量,反应的中和热是
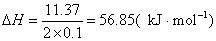
❷根据实验Ⅱ数据得:
Q=4.18×(150+150)×(26.8-20)=8527(J)
生成(1×0.15)mol水时放出热量8.527 kJ,中和热是
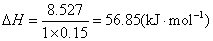
答 实验Ⅰ和Ⅱ的中和热都是56.85kJ·mol-1。根据实验知道,用相同浓度、相同体积的酸跟碱中和时,测得的温度和热量有如下规律:
❶溶液温度升高度数与所用酸与碱的体积多少无关;
❷所用酸与碱浓度愈大,反应放出热量愈多。例 3 0.11mol· L-1 NaOH溶液100mL和0.1mol·L-1盐酸100 mL混合后能放出多少热量?混合后溶液温度升高多少?
解 由题意知氢氧化钠过量,以HCl计算。设该反应放出热量为Q:
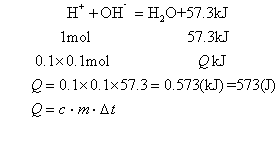
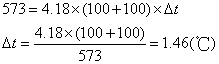
答 能放出573J热量,溶液温度升高1.46℃。
☚ 求反应热 键能的计算 ☛
- 櫠是什么意思
- 櫡是什么意思
- 櫢是什么意思
- 櫢檽是什么意思
- 櫣是什么意思
- 櫤是什么意思
- 櫥是什么意思
- 櫦是什么意思
- 櫧是什么意思
- 櫧子是什么意思
- 櫨是什么意思
- 櫩是什么意思
- 櫩庑是什么意思
- 櫩廡是什么意思
- 櫪是什么意思
- 櫪㯕是什么意思
- 櫫是什么意思
- 櫬是什么意思
- 櫭是什么意思
- 櫭仔是什么意思
- 櫭涸板是什么意思
- 櫮是什么意思
- 櫯是什么意思
- 櫰是什么意思
- 櫰香是什么意思
- 櫰香根是什么意思
- 櫱是什么意思
- 櫲是什么意思
- 櫳是什么意思
- 櫳門是什么意思
- 櫳門兒是什么意思
- 櫴是什么意思
- 櫵是什么意思
- 櫶是什么意思
- 櫷是什么意思
- 櫸是什么意思
- 櫸柳是什么意思
- 櫹是什么意思
- 櫹椮是什么意思
- 櫹槮是什么意思
- 櫺是什么意思
- 櫺床是什么意思
- 櫺星門是什么意思
- 櫺槛是什么意思
- 櫺檻是什么意思
- 櫺牀是什么意思
- 櫺軒是什么意思
- 櫻是什么意思
- 櫻桃是什么意思
- 櫻桃口是什么意思
- 櫻桃宴是什么意思
- 櫻桃煎是什么意思
- 櫻脣是什么意思
- 櫼是什么意思
- 櫼头到脚是什么意思
- 櫼头对脚是什么意思
- 櫼子是什么意思
- 櫼枊是什么意思
- 櫼栌是什么意思
- 櫼队是什么意思