氢化物的还原性
氢化物的还原性qinghuawu de huan yuanxing
除氟化氢外,其他非金属元素的氢化物都有还原性,元素的非金属性越强、电负性越大,则吸引电子能力越强,故难失电子,还原性差; 反之,则还原性强。可根据元素周期表判断它们还原性的强弱:
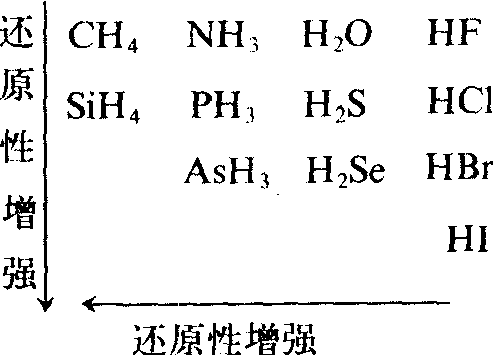
这些氢化物的还原性表现在:
❶与氧气、氯气等较活泼的非金属单质作用,例如:
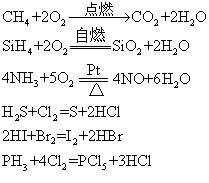
❷ 与氧化性酸反应,例如:
2HBr+H2SO4(浓)=Br2+SO2↑+2H2O
6HI+HClO3=3I2+HCl+3H2O
❸ 与氧化性强的金属阳离子作用,例如:
2FeCl3+2HI=2FeCl2+I2+2HCl
6AgNO3+AsH3+3H2O=H3AsO3+6HNO3+6Ag
❹与氧化性强的含氧酸盐作用,例如:
2KMnO4+16HCl
=2KCl+2MnCl2+5Cl2↑+8H2O
2KMnO4+5H2S+3H2SO4
=K2SO4+2MnSO4+5S↓+8H2O
❺与其他氧化剂的作用,例如:
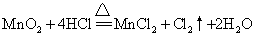
☚ 氧化性酸 含氧酸盐的氧化性和还原性 ☛
- 晒不燥是什么意思
- 晒书是什么意思
- 晒书人是什么意思
- 晒书会是什么意思
- 晒书堂是什么意思
- 晒书堂文集是什么意思
- 晒书堂集是什么意思
- 晒书秋日晚,洗药石泉香。是什么意思
- 晒书节是什么意思
- 晒了是什么意思
- 晒了一天的黄瓜——蔫了是什么意思
- 晒伏是什么意思
- 晒伤是什么意思
- 晒佛节是什么意思
- 晒信是什么意思
- 晒儿粮是什么意思
- 晒冬田是什么意思
- 晒卡族是什么意思
- 晒印照片是什么意思
- 晒印镊子是什么意思
- 晒去是什么意思
- 晒友是什么意思
- 晒发使干是什么意思
- 晒台是什么意思
- 晒品是什么意思
- 晒嗉子是什么意思
- 晒图是什么意思
- 晒图员是什么意思
- 晒图复印是什么意思
- 晒图机是什么意思
- 晒图纸是什么意思
- 晒地皮是什么意思
- 晒场是什么意思
- 晒场上泼水银——无孔不入是什么意思
- 晒场作业机械是什么意思
- 晒场挖不出黄鳝是什么意思
- 晒坛是什么意思
- 晒坝是什么意思
- 晒坝头
 雀雀儿——响不得是什么意思
雀雀儿——响不得是什么意思 - 晒坪是什么意思
- 晒垡是什么意思
- 晒垫是什么意思
- 晒士是什么意思
- 晒太暖是什么意思
- 晒太阳是什么意思
- 晒客是什么意思
- 晒密是什么意思
- 晒寒地是什么意思
- 晒尸是什么意思
- 晒尸房是什么意思
- 晒工资是什么意思
- 晒席是什么意思
- 晒干是什么意思
- 晒干、风干的果品是什么意思
- 晒干儿是什么意思
- 晒干或蜜渍的果实是什么意思
- 晒干油是什么意思
- 晒干瓢是什么意思
- 晒干的爆竹是什么意思
- 晒干的草是什么意思