妊娠生理与计划生育
妊娠期计算,如自排卵日算起为266日;自末次月经第一日算起,则为280日。妊娠期间母体各系统发生一系列变化,以适应胎儿生长需要。故在计划生育实施和科研工作中,须对妊娠生理深入了解,才能提高计划生育质量,减少副作用,避免并发症。孕妇如须终止妊娠,在不同孕期,应根据妊娠生理变化选择最适当的措施,以获得满意效果。中止中期妊娠以不超过妊娠6个月为宜。妊娠6个月内母体及胎儿的生理变化如下:
母体生理变化 主要表现在生殖、循环、消化、泌尿系统方面的变化。
生殖系统 子宫由于肌纤维肥大,纤维组织与血管增生,子宫壁迅速增厚、增长、变软,妊娠6周子宫呈梨形,12周成圆球形,后成卵圆形。因盆腔左侧有乙状结肠,故子宫上升到腹腔时常略向右转。妊娠16周子宫壁最厚,约2~2.5cm,以后子宫逐渐扩张,子宫壁也变薄,足月时仅0.5~1cm。早期妊娠时子宫增长不对称,底部增长最快,胎盘附着处更快。6周时子宫呈不对称增长,柔软也不一。由于肌纤维敏感性增加,子宫常有间歇性收缩。子宫峡部于妊娠3月时逐渐伸展,质软。子宫前屈或后屈位时,人工流产需谨慎,以免穿通峡部。子宫颈也变软,呈紫蓝色。
卵泡发育及排卵在妊娠期均暂停。一侧卵巢含有妊娠黄体。妊娠4周时黄体功能达高峰。5周后绒毛膜促性腺激素(hCG)量虽不断上升,卵巢合成甾体激素能力开始下降,但整个妊娠期,黄体仍具有分泌少量孕酮的功能。排卵后或妊娠期黄体增大,直径可达4~6cm,甚至形成囊肿达10~12cm,充满棕色或黄色液体,除非破裂或扭转,不需手术。黄体囊肿每能自行消退,人工流产扎管时也不必切除。妊娠期卵巢间质细胞黄素化反应过度,能形成实质性黄素瘤,甚至能引起暂时性雄性化症状,但并非真正肿瘤,分娩后也能自行退化。妊娠期卵巢表面蜕膜样反应,能形成微小息肉或肉芽,触之易出血,好像新撕裂的粘连,这现象也能见于子宫后壁浆膜或盆腔内外器官上,有时在扎管中能遇到。
妊娠期,雌、孕激素,胎盘生乳素,胰岛素,皮质醇,垂体生乳素等使乳腺发育完善。乳房在早期有胀感,怀孕第二月起,乳房开始增大。由于腺体增生可扪到很多小结节。乳头增大、色深、易勃起。乳晕着色较深,并有肥大隆起的皮脂腺,分布在乳头周围。妊娠4个月后可有黄色初乳分泌。妊娠期,高水平的雌激素与孕激素抑制了下丘脑催乳素抑制因子,致催乳素分泌逐渐升高。早孕时血清催乳素平均为75ng/ml,中期约116ng/ml,晚期则超过200ng/ml。这些激素变化促进了乳腺导管与小叶腺泡系统显著增长,在妊娠期已能生乳,但乳汁分泌甚少。可能是雌激素通过对乳腺实质细胞的抑制,阻止了乳汁的生成。孕酮则抑制核酸和乳清蛋白合成。因妊娠前半期乳房已处于准备就绪的分泌状态,所以孕期超过16周终止妊娠时,即有乳汁生成,有时需要回乳。
循环系统 妊娠早期血循环量开始上升,妊娠中期增加可达30%,其中血浆增加40%,血细胞增加20%,造成生理性血液稀释。因此,妊娠期血红蛋白在10g%以下时才成立贫血。孕妇血液中凝血因子活力增高,常处于高凝状态。纤维蛋白原可增加50%,致血沉加速,故妊娠期血沉检查无诊断价值。纤维素降解物常略升高,前纤维溶解素明显增加。此外,羊水及胎盘组织中含有大量凝血活素,若进入循环,可产生血管内凝血症状与继发纤溶性凝血障碍。中期妊娠引产时,如月份较大,要特别注意。妊娠期白细胞增加,约为8000~10,000/mm3。以嗜中性细胞为主,应和感染或炎症区别。天花粉引产也常引起白细胞上升。妊娠期,脉搏每分钟增加10~15次。妊娠时收缩压无明显上升。由于外周阻力下降,舒张压则略下降。上半身静脉压无改变,下肢静脉压则自10mmHg上升到30mmHg。
消化系统 早期常出现食欲减退、恶心、呕吐等症状。于妊娠12周后逐渐消失。由于肠胃系统呈弛缓状态,贲门松弛,胃内容物能倒流入食道而致胃部灼热感,并常有胃胀气或便秘。此外,由于子宫增大,阑尾逐渐向上方推移,对妊娠期急性阑尾炎诊断有一定重要性。妊娠时肝组织活检与电镜检查均未发现异常,但有些肝功能试验可出现变化。碱性磷酸酶活力可增加两倍,白蛋白/球蛋白比例下降,肝实质细胞分泌磺溴酞入胆汁的功能下降。少数孕妇麝香草酚浊度、硫酸锌浊度、脑磷脂絮状试验呈阳性反应,有时SGPT上升,提示有肝功能改变。常无自觉症状。故对中期妊娠引产孕妇或所用药物能影响肝功能者,须作肝功能检查并严密观察肝功能变化。
泌尿系统 早期尚在盆腔内的子宫易压迫膀胱,常有尿频。此期肾血流量与肾小球滤过率均已增加,后者可达50%。体位能明显影响肾血流量与肾小球滤过率,因此孕妇夜间尿量多于白天。有1/6的孕妇饭后能出现糖尿,是由于葡萄糖的肾小球滤过率增加,而肾小管的再吸收率未增加。肌酐、尿素的排泄量增加,并有少量蛋白自尿排出,均属生理现象。妊娠期输尿管平滑肌松弛而扩张,常致尿潴留,因而易发生感染。
胎儿变化 卵子受精后2周内(末次月经后4周)称为受精卵。受孕后3~4日,受精卵中开始积聚液体,形成囊胚腔。在受精后第8~9日,受精卵植入子宫内膜(即着床),滋养层增生,日后发育成胎盘。末次月经后5~8周内,称为胚胎,各主要器官已形成,8周后称为胎儿,此时各器官继续发育成熟。
第一月末(末次月经后4周),头部和躯体呈直角,因此顶臀长度不能代表胚胎的真正长度。出现肢芽,尾部突出;第二月末,长约2.5cm,重1g。头部特大,相当于躯体的一半。眼、耳、鼻、口已能认出。肢芽伸长,指、趾明显。尾部几乎消失,外生殖器已出现;第三月末,生长迅速,身长已达8~9cm,重15~30g。头部为胎儿全身的1/3。指甲、趾甲生出,外生殖器已显示性征。小肠有蠕动并能吸收葡萄糖;第四月末,身长15~17cm,重约100~120g。出现头发,能听到胎心搏动,孕妇能感到四肢运动,大肠内有胎粪;第五月末,身长25cm,体重250~300g。皮肤呈暗红色,有胎毛,开始吞咽活动;第六月末,身长28~32cm,重600~700g。皮肤有皱纹,皮下有少许脂肪出现。有类似呼吸动作,但出生后很难存活。
通常以胎儿身长与体重估计胎龄。妊娠早期,胎儿增长较后期迅速。体重则与孕妇营养及胎盘功能有关。用下列公式计算各月份胎儿的平均身长和体重,对于妊娠3个月以上者,还比较符合。
妊娠3~5个月胎儿身长(cm)=月数2
体重(g)=月数3×2
妊娠6~10个月胎儿身长(cm)=月数×5
体重(g)=月数3×3
胎盘与蜕膜 胎盘、蜕膜及胎盘的激素与抗原物质对于维持妊娠和胚胎发育至为重要,因而也是计划生育研究中的重要环节。
蜕膜 排卵后,因受孕激素影响,分泌型内膜逐渐呈现蜕膜样反应,以备受精卵着床。在受精卵植入后数天,蜕膜反应才全部完成。蜕膜分基底层、海绵层、致密层,后两层为功能层。孕三月末,蜕膜层增厚可达10mm。抗早孕时,绒毛及蜕膜有时堵塞在子宫口,不易排出。受精卵着床后,着床部位的蜕膜称底蜕膜。妊娠8周时,绒毛组织的发育已集中在底蜕膜处生长。覆盖在受精卵上的蜕膜,称包蜕膜,将受精卵与子宫腔隔开。在孕二月时,包蜕膜仅由一层蜕膜细胞及上皮细胞组成,直接与绒毛膜贴近。子宫其余部分蜕膜称真蜕膜。妊娠早期,受精卵在子宫腔一侧发育,包蜕膜和真蜕膜之间留有空隙。药物抗早孕时,胚胎和包蜕膜虽排出,真蜕膜与底蜕膜常残留,引起流产后阴道流血时间较长。妊娠4个月后,包蜕膜与真蜕膜逐渐接近,终至粘连而封闭子宫腔。由于胚胎发育,真蜕膜受压,逐渐变薄。早孕期蜕膜坏死属正常现象,故在流产后刮出内膜检查时,常能发现有内膜坏死。
胎盘 早期囊胚壁表面布满绒毛,从蜕膜血窦中吸收营养。底蜕膜处绒毛将发育成为丛密绒毛膜。包蜕膜部绒毛膜因缺乏营养,绒毛逐渐退化,成为平滑绒毛膜。丛密绒毛膜的绒毛大部分是游离的,称为游离绒毛。绒毛之间有间隙,称绒毛间隙。螺旋动脉与静脉穿过蜕膜板开口于绒毛间隙,使间隙充满母血。绒毛则浸在母血中,交换气体、吸收营养、并排出废物。另有少数绒毛长入底蜕膜成为固定绒毛。妊娠2~3月时,胎盘占子宫腔面积1/3。4个月时,胎盘是半球形,约占子宫腔一半。早孕时,胚胎小较易排出;但胎盘尚未形成,故不易完整排出,而常部分或大部遗留在子宫腔内,应密切注意。
胎盘激素及非激素的胎盘抗原 胎盘能合成大量物质,主要为各种激素与酶。胎盘的蛋白激素有绒毛膜促性腺激素与胎盘生乳素,测定这些激素可以协助诊断妊娠。胎盘甾体激素性能和母体合成者相同。胎盘酶系统种类繁多,和胎儿酶系统互相配合可合成大部分甾体激素。
人绒毛膜促性腺激素(hCG):在孕妇血和尿中都大量存在,故能用生物法或免疫法作测定以诊断早孕。非妊娠期,hCG出现于血或尿中属病理现象,提示有肿瘤组织分泌这种激素。hCG的生物活性和黄体生成素(LH)有类似处。hCG主要由滋养层合体细胞分泌,分子量为45,000~50,000道尔顿(dalton,一个dalton等于氧原子体积的1/16),是一种糖蛋白,由一蛋白核心及若干糖分子侧链组成。hCG的生物活力约每毫克相当于12,000~18,000IU。即使两种hCG的氨基酸量完全相同,如涎酸量不同,则生物活力就有很大差别。涎酸量低,生物活力也低,但免疫活力不受影响。
(1) hCG分子的两个组成部分: hCG和垂体糖蛋白激素(FSH、LH、TSH)一样,均由α-亚基与β-亚基组成。α-亚基的分子量为15,000~20,000dalton,氨基酸数量在89~92之间。β-亚基的分子量为25,000~30,000dalton,氨基酸数量在147~149之间。被分解的两个亚基几无生物活力,但重新组合后,可恢复原来hCG生物活力的80%。hCG亚基并能和LH亚基或促甲状腺激素(TSH)亚基组合。组合后激素的活力性质由β-亚基决定,因只有β-亚基能特异性地与靶器官上的受体相结合。
由于hCG和各种垂体糖蛋白激素的α-亚基具有相同的氨基酸排列,故hCG的α-亚基抗血清和上述激素及其α-亚基都能发生交叉反应。相反,hCG的β-亚基抗血清则仅对hCG及其β-亚基发生反应,而对LH及其β-亚基不发生反应。因此就可利用hCG的β-亚基抗血清的特异性来测定hCG而不被LH所干扰,对诊断早孕更为准确。
(2)妊娠与hCG:在受孕后2~8日,血浆中就能测出hCG,并很快上升。在40~90日时,血浆hCG为70~200IU/ml,以后很快下降。在中期与晚期妊娠,hCG量仅为高峰时的10%。通常在月经延期3日后,就能在尿中测出hCG,约625IU/L。妊娠40日时,尿hCG达5,000IU/L。在60~70日出现高峰,达8~32万IU/L,个别孕妇能达256万IU/L,但高峰不超过10日,以后就很快下降到1~2万IU/L。胎盘分泌的hCG能维持卵巢黄体到早孕的6~8周,使黄体能继续分泌孕酮,以维持已着床的胚胎,以后胎盘则成为分泌孕酮的主要器官。
人胎盘生乳素(hPL):是由191个氨基酸的单链组成的蛋白质。分子量为21,000~23,000。hPL和人生长激素(hGH)在生化方面的关系极为密切。hPL系由合体滋养层细胞分泌。hPL对啮齿动物有促黄体生成作用,在人类hPL的泌乳作用不明显,但在组织培养中能刺激乳腺上皮细胞合成酪蛋白、乳白蛋白与乳珠蛋白。hPL与hGH一样,能增加蛋白的合成作用,造成正氮平衡。hPL并有脂解作用,释放出游离脂肪酸,肌组织将其摄取,而将过剩的葡萄糖运给胎儿。一般在末次月经后5~6周,在血浆中可测出hPL。开始时上升缓慢,自15~30周即快速上升。34周达高峰,约7.75~10.6μg/ml,以后维持到分娩。其分泌量同胎盘体积成正比。
雌激素: (1)胎儿-胎盘单位: 胎儿与胎盘各缺乏一些合成甾体所必需的酶,但胎盘缺乏的酶却能在胎儿中找到,反之亦然。如此,胎儿与胎盘功能相结合,就能合成大部,甚至全部具有生物活力的甾体激素。妊娠期雌激(E2)仍由卵巢分泌,但自第7周起,已由胎盘分泌。雌二醇很快就上升,在第10周已7倍于月经周期黄体期高峰的浓度。在血流中E2主要是游离的。母体的硫酸脱氢表雄酮(DHAS)是形成雌二醇的主要前体。在妊娠9周前,血浆中游离雌三醇(E3)仅50pg/ml。三个月末,E3量也仅为E2的7%。胎儿-胎盘单位产生的E3,有86%来自胎儿的DHAS,4%来自胎儿的E2,仅10%来自母体的DHAS。胎血中的DHAS必须先在胎儿肝脏中羟化为硫酸16α羟脱氢表雄酮(16α羟DHAS),然后进入胎盘,才能转变为E3。E2与E3的半衰期都是20分钟。
(2) 尿中雌激素浓度: 妊娠晚期尿中有大量E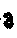 约占尿中雌激素总量的90%,而雌酮(E1)和雌二醇(E2)的量很少。尿中E
约占尿中雌激素总量的90%,而雌酮(E1)和雌二醇(E2)的量很少。尿中E 都和醛糖酸或硫酸联结,通常要经过酸解才能进行测定。尿E3平均值在妊娠8~12周为1~2mg/24小时,28周为10.1mg/24h。
都和醛糖酸或硫酸联结,通常要经过酸解才能进行测定。尿E3平均值在妊娠8~12周为1~2mg/24小时,28周为10.1mg/24h。
(3) E3的生理作用: 在动物试验中,雌二醇对受精卵植入是必需的。一旦植入,则必须E3才能维持妊娠。植入前给动物注射E3抗血清,不能阻止植入。注入E2抗血清则能阻止植入。在植入后,给动物注射E2抗血清不发生作用。如注入E3抗血清,则能使胚胎吸收,终止妊娠。E3能与子宫肌细胞的雌激素受体结合,使E2与受体结合的比例下降,因而使子宫对催产素不敏感。当E2与E3在等克分子浓度时,受体上50%的E2能被E3取代。应用药物中期妊娠引产时,如孕妇血或尿E3下降,有利于引产成功。
孕酮: 妊娠8周后孕酮主要由胎盘的合体滋养层细胞分泌。脐静脉中孕酮高于脐动脉,提示孕酮不但进入胎儿循环,而且胎儿还利用孕酮。进入胎体的孕酮量为84mg/日,在胎儿肝与肾上腺中转变成皮质酮、皮质醇、17α羟孕酮等物质。孕酮进入母体后很快就消失,消失曲线呈两个坡度。第一次半衰期为6分钟,第二次半衰期为95分钟,提示孕酮系分布在两个区域内。一部分在血浆中很快被清除,另一部分可能在脂肪或体液中,故逸出较慢。孕酮最后代谢为孕二醇,但仅有10~15%自尿排出。
(1) 孕妇血清孕酮浓度: 末次月经后第4周,受精卵着床时,血清孕酮相当于月经黄体期水平。用放射免疫法测定,可达13.8ng/ml。以后陆续上升,7周可达19.4~24.5ng/ml,通常认为在妊娠7周割除黄体可导致孕酮下降而流产;在9周时,则仅使孕酮暂时下降,但不发生流产,自8~9周起,滋养层能分泌足够的孕酮以维持妊娠。
(2) 孕酮的生理作用: 雌激素和孕酮的协同作用,促进了子宫生长所需的蛋白合成。受精卵在子宫内如同异物易引起收缩。对降低子宫的应激性,孕酮可能起了主要的镇静作用。孕酮能和肾小管中醛固酮蛋白受体结合,对醛固酮起了竞争抑制作用,使钠丧失。于是肾素-血管紧张素系统受刺激,醛固酮分泌增加,克服了暂时性钠丧失。妊娠期大量孕酮导致醛固酮分泌上升,以取得钠平衡。虽然孕酮能刺激子宫与乳腺发育,但对机体代谢是分解性的。注射孕酮后,尿素氮排泄量增加,说明蛋白分解增加。孕酮增加到一定量后,尿素氮丧失不再增加。所以妊娠期的蛋白分解是有限的。
hCG人绒毛膜促性腺激素
hPL人胎盘生乳素
E3雌三醇
P孕酮
血中胎盘激素的变化
妊娠特异性β1糖蛋白: 简称PSβ1G或SP1。孕期血浆中有多种蛋白质,有的是特异性的,如hCG、hPL与SP1。它们随着妊娠进展而增加,在非孕期血浆中量极少。有的蛋白质虽和妊娠有关,但在非孕期血浆中量也相当大,如结合甾体β球蛋白等。SP1由合体滋养层细胞分泌,分子量为90,000道尔顿,半衰期约30小时。受精卵植入后,SP1进入母体循环,最早在受孕后7日在血中就能测出。以后则SP1逐渐上升,34周达高峰,约200μg/ml,并维持在这水平。脐血中SP1较母血中低1000倍,羊水中较母血中低100倍。无脑儿羊水中SP1和正常羊水中浓度无区别。在尿中,SP1最早在受孕后22日才能测出,故不及其他诊断方法灵敏。由于SP1对LH无交叉反应,故如用作抗原,可能发展成为避孕或抗早孕的制剂。
- 欢乐的歌声是什么意思
- 欢乐的气氛是什么意思
- 欢乐的气氛很盛是什么意思
- 欢乐的泪水是什么意思
- 欢乐的源泉是劳动是什么意思
- 欢乐的神色是什么意思
- 欢乐的程度是什么意思
- 欢乐的聚会是什么意思
- 欢乐的舞蹈是什么意思
- 欢乐的除夕是什么意思
- 欢乐相伴,直到永远是什么意思
- 欢乐祥和是什么意思
- 欢乐租车有限公司是什么意思
- 欢乐窑是什么意思
- 欢乐笑谑是什么意思
- 欢乐美好的时光过得快是什么意思
- 欢乐而美好的短暂时刻是什么意思
- 欢乐荣华是什么意思
- 欢乐融洽是什么意思
- 欢乐行走的样子是什么意思
- 欢乐过度化为悲是什么意思
- 欢乐适意是什么意思
- 欢乐颂是什么意思
- 欢乐颂 [德国]席勒是什么意思
- 欢乐(娱)嫌夜短,寂寞恨更长是什么意思
- 欢乐)(何其芳)是什么意思
- 欢乐,喜悦是什么意思
- 欢些是什么意思
- 欢亮是什么意思
- 欢从是什么意思
- 欢仙客是什么意思
- 欢休是什么意思
- 欢会是什么意思
- 欢会和别离是什么意思
- 欢会和离别是什么意思
- 欢会方别离,戚戚忧虑并。是什么意思
- 欢会歌 [希腊]忒奥克里托斯是什么意思
- 欢会结束,彼此分离是什么意思
- 欢传扬是什么意思
- 欢伯是什么意思
- 欢伯肾人是什么意思
- 欢佬啊是什么意思
- 欢信是什么意思
- 欢儿是什么意思
- 欢全是什么意思
- 欢公测是什么意思
- 欢动是什么意思
- 欢动宸严,宴开鹤禁,生朝和气。是什么意思
- 欢势是什么意思
- 欢勒也是什么意思
- 欢勒脚是什么意思
- 欢卞鼓舞是什么意思
- 欢友是什么意思
- 欢叫是什么意思
- 欢叫雀跃是什么意思
- 欢台吉是什么意思
- 欢叹是什么意思
- 欢合是什么意思
- 欢君是什么意思
- 欢呀是什么意思